Die Nachverfolgung der Deckschichtbildung unter verschiedenen klimatischen Bedingungen oder auch die Charakterisierung des aktuellen Zustands eines Bauteils oder einer Konstruktion aus verzinktem Stahl ist bisher nicht einfach realisierbar gewesen. Aufgrund der sehr geringen Korrosionsraten sind dafür langwierige Versuchsprogramme und aufwändige Untersuchungen an den Proben notwendig. Aus praktischer und wissenschaftlicher Sicht ergeben sich jedoch sehr interessante Fragestellungen, für die sich die Korrosionsdiagnostik mit elektrochemischen Methoden unter Verwendung von gel-artigen Elektrolyten sehr gut einsetzen lässt. Der Vorteil liegt auch hier in der einfachen Umsetzung der elektrochemischen Messungen und der minimal-invasiven Vorgehensweise, durch die sich der Deckschichtzustand während der Analyse nicht wesentlich verändert. Dies kann verdeutlicht werden, wenn man Flüssig-Elektrolyte und Gel-Elektrolyte gleicher chemischer Zusammensetzung gegenüberstellt. Abbildung 11 zeigt den Verlauf von Polarisationswiderständen in Abhängigkeit des verwendeten Elektrolyten von einer verzinkten Stahlprobe mit einer atmosphärisch gebildeten Deckschicht.
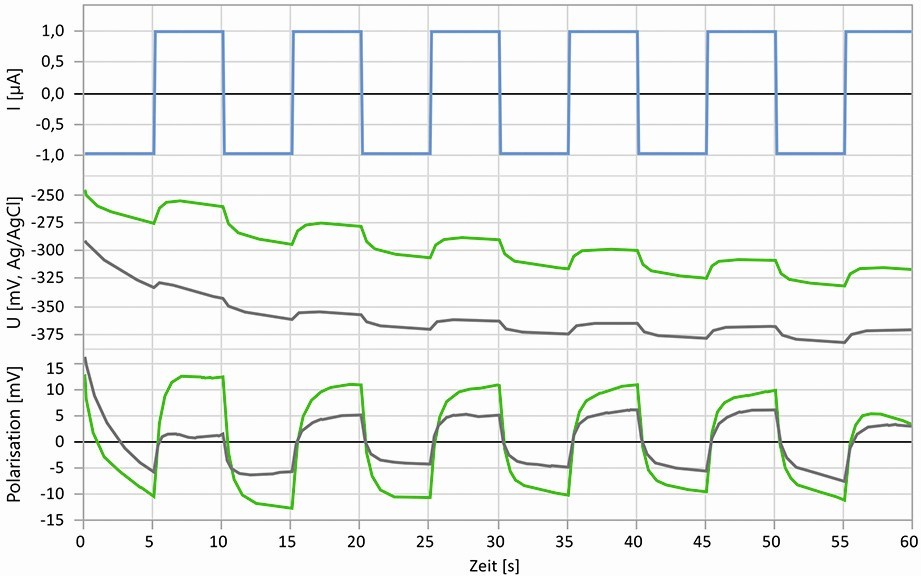 Abb. 10: Minimal-invasive galvanostatische Pulsmessungen über 60 Sekunden an unbehandeltem (grau) Stahl und Stahl bei Auslagerung in VCI-Atmosphäre (grün), oben: Anregung mit Pulsstrom, Mitte: Potentialverläufe, unten: Polarisationsverläufe
Abb. 10: Minimal-invasive galvanostatische Pulsmessungen über 60 Sekunden an unbehandeltem (grau) Stahl und Stahl bei Auslagerung in VCI-Atmosphäre (grün), oben: Anregung mit Pulsstrom, Mitte: Potentialverläufe, unten: Polarisationsverläufe
Die Polarisationswiderstände wurden mit der in Abbildung 10 gezeigten Methode des galvanostatischen Pulsens ermittelt, durch die nur eine sehr geringe Beeinflussung der Oberfläche erfolgt. Nach Kontakt mit den flüssigen Elektrolyten sinkt der Polarisationswiderstand innerhalb weniger Minuten von etwa 200 kΩcm2 auf 50 kΩcm2, wohingegen er bei den Gel-Elektrolyten deutlich länger konstant hoch bleibt und dadurch die elektrochemische Charakterisierung dieses Zustands über einen längeren Zeitraum ermöglicht. Der Grund dafür liegt in der Eigenschaft des Gel-Elektrolyten, einen dünnen Elektrolytfilm an der Oberfläche auszubilden, wodurch sich die Korrosionsprodukte deutlich langsamer lösen und ihr Abtransport von der Oberfläche durch das Gel-Netzwerk gehemmt ist. Dieser Zustand liegt näher an den Bedingungen, die an einer Metalloberfläche in einer feuchten Atmosphäre auftreten. Auch hier ist in den meisten Fällen ein dünner Elektrolytfilm an der Oberfläche vorhanden, der einen Abtransport von Korrosionsprodukten unterdrückt.
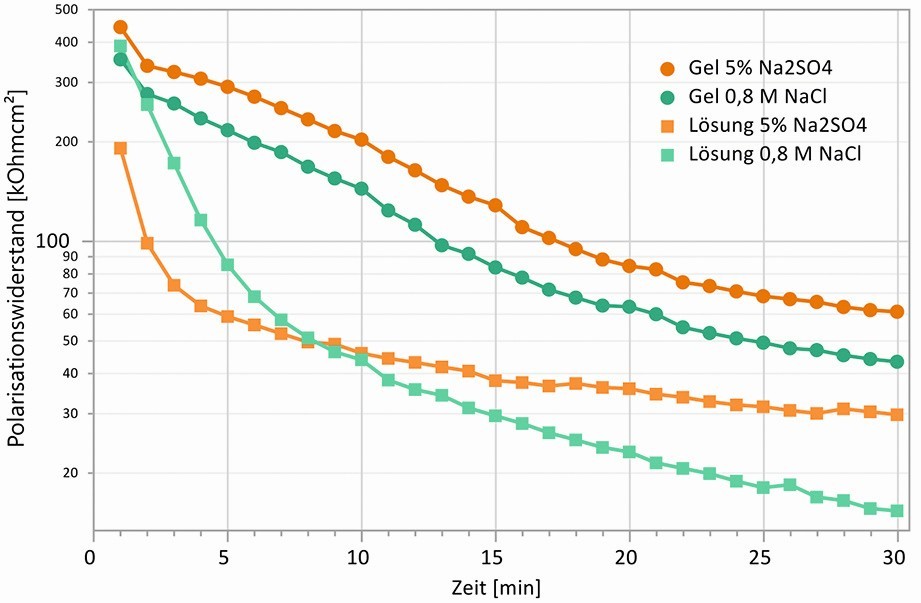 Abb. 11: Verläufe von Polarisationswiderständen über 30 min bei Kontakt mit Gel- und Flüssig-Elektrolyten, verzinkter Stahl mit atmosphärisch (C2 Stadt-Atmosphäre) gebildeter Deckschicht
Abb. 11: Verläufe von Polarisationswiderständen über 30 min bei Kontakt mit Gel- und Flüssig-Elektrolyten, verzinkter Stahl mit atmosphärisch (C2 Stadt-Atmosphäre) gebildeter Deckschicht
Auf diese Art und Weise wurden im Laufe der letzten Jahre bereits zahlreiche Untersuchungen durchgeführt. In [23] wird z. B. durch Messungen mit Gel-Elektrolyten die Aufbau- und Stabilisierungsphase von Zink-Proben unter verschiedenen atmosphärischen Bedingungen beschrieben. Abbildung 12 zeigt ein wichtiges Ergebnis dieser Untersuchungen.
Beeindruckend ist, dass sich bei idealen, abwechselnd feucht-trockenen Bedingungen die Deckschicht innerhalb der ersten 2–3 Wochen ausbilden kann und dann bereits in eine Stabilisierungsphase übergeht, in der die Korrosionsstromdichten sehr niedrig sind. Dagegen bleibt sie unter trockenen Bedingungen (33 % relative Feuchte) unfertig ausgebildet und unter feuchten Bedingungen (96 % relative Feuchte) ebenfalls konstant, jedoch deutlich weniger beständig. Die Polarisationswiderstände für eine stabile Deckschichtphase unter der C2-Atmosphäre liegen bei deutlich über 100 kΩcm2 (entspricht deutlich weniger als 0,08 µA/cm2), wohingegen unter den Konstantklimaten weitaus geringere Polarisationswiderstände ermittelt werden (0,4 µA/cm2 entsprechen ca. 26 kΩcm2). Die Verwendung von Gel-Elektrolyten zur Bestimmung von Deckschichtwiderständen an Zinküberzügen wird gegenwärtig an der BAM Bundesanstalt für Materialforschung und -prüfung (Berlin) in Rahmen der Forschungsinitiative WIPANO (Wissenstransfer durch Patente und Normen) des BMWi untersucht [29], um einen Normentwurf für ein Prüfverfahren vorzubereiten.
![Abb. 12: Verläufe der momentanen Korrosionsstromdichten, bestimmt durch Versuche mit gel-artigen Elektrolyten, von unterschiedlich ausgelagerten Zink-Proben, Babutzka et al. [23] Abb. 12: Verläufe der momentanen Korrosionsstromdichten, bestimmt durch Versuche mit gel-artigen Elektrolyten, von unterschiedlich ausgelagerten Zink-Proben, Babutzka et al. [23]](/images/stories/Abo-2022-02/gt-2022-02-0074.jpg) Abb. 12: Verläufe der momentanen Korrosionsstromdichten, bestimmt durch Versuche mit gel-artigen Elektrolyten, von unterschiedlich ausgelagerten Zink-Proben, Babutzka et al. [23]
Abb. 12: Verläufe der momentanen Korrosionsstromdichten, bestimmt durch Versuche mit gel-artigen Elektrolyten, von unterschiedlich ausgelagerten Zink-Proben, Babutzka et al. [23]
![Abb. 13: Veränderung von Polarisationswiderständen unterschiedlicher Verzinkungen auf Stahl in einem Kurzzeitkorrosionstest der Automobilindustrie, Daten aus [30] Abb. 13: Veränderung von Polarisationswiderständen unterschiedlicher Verzinkungen auf Stahl in einem Kurzzeitkorrosionstest der Automobilindustrie, Daten aus [30]](/images/stories/Abo-2022-02/thumbnails/thumb_gt-2022-02-0075.jpg) Abb. 13: Veränderung von Polarisationswiderständen unterschiedlicher Verzinkungen auf Stahl in einem Kurzzeitkorrosionstest der Automobilindustrie, Daten aus [30] Mit Blick auf das Verhalten von verzinktem Stahl unter atmosphärischen Bedingungen stellt sich häufig die Frage, ob dieses Verhalten durch Tests in künstlichen, meist verschärften Klimaten nachgestellt oder sogar beschleunigt werden kann. Auch für diese Fragestellung lässt sich die Methodik sehr gut einsetzen. Es ist zwar kein kontinuierliches Monitoring über den gesamten Testverlauf möglich, jedoch kann man nach bestimmten Testintervallen relativ einfach Messungen an den zuvor ausgelagerten Proben vornehmen und den momentanen Oberflächenzustand (Schutzvermögen der Deckschicht) damit sehr gut dokumentieren. In einer Arbeit von Killik wurden mit dieser Herangehensweise verschiedene Verzinkungen auf Stahl während der Auslagerung in einem typischen Kurzzeitkorrosionstest der Automobilindustrie untersucht [30] und mit Feldbauteilen verglichen. Abbildung 13 zeigt den zeitlichen Verlauf von Polarisationswiderständen verschiedener Verzinkungen im Testverlauf. Die Messungen erfolgten in der ersten Woche nach bestimmten Einzelzyklen des Tests und im Langzeitbereich nach 1, 2, 4 und 8 Wochen. Die einzelnen Verzinkungen liegen auf unterschiedlichen Leveln, ohne jedoch eine ausgeprägte Tendenz zur Erhöhung des Deckschichtwiderstands aufzuweisen. Die Passivierungen machen sich im Testverlauf stark bemerkbar, indem sie die Widerstände erhöhen und den Abfall auf niedrige Werte teilweise verzögern. Die normale Feuerverzinkung korrodiert in diesem Test am stärksten (geringste Widerstände), hat allerdings auch eine höhere Überzugsdicke und zeigt am Ende der Testzeit Rotrost und einen Einbruch des Polarisationswiderstandes. Die galvanisch abgeschiedenen Überzüge Zn-Fe und Zn-Ni weisen höhere Widerstände auf, jedoch ist die Korrosion trotzdem noch so stark (und die Überzugsdicke im Verhältnis geringer), dass sie im Testverlauf ebenfalls zum Rotrost und damit zum starken Einbruch der Widerstände führt. Für alle getesteten Verzinkungsvarianten ist in diesem Kurzzeitkorrosionstest keine Deckschichtbildung nachweisbar, wie sie unter atmosphärischen Bedingungen beobachtet wird. Dies liegt maßgeblich an den verschärften Prüfbedingungen (hohe Temperaturen, hohe Befeuchtungsdauern, starke Salzbelastung).
Abb. 13: Veränderung von Polarisationswiderständen unterschiedlicher Verzinkungen auf Stahl in einem Kurzzeitkorrosionstest der Automobilindustrie, Daten aus [30] Mit Blick auf das Verhalten von verzinktem Stahl unter atmosphärischen Bedingungen stellt sich häufig die Frage, ob dieses Verhalten durch Tests in künstlichen, meist verschärften Klimaten nachgestellt oder sogar beschleunigt werden kann. Auch für diese Fragestellung lässt sich die Methodik sehr gut einsetzen. Es ist zwar kein kontinuierliches Monitoring über den gesamten Testverlauf möglich, jedoch kann man nach bestimmten Testintervallen relativ einfach Messungen an den zuvor ausgelagerten Proben vornehmen und den momentanen Oberflächenzustand (Schutzvermögen der Deckschicht) damit sehr gut dokumentieren. In einer Arbeit von Killik wurden mit dieser Herangehensweise verschiedene Verzinkungen auf Stahl während der Auslagerung in einem typischen Kurzzeitkorrosionstest der Automobilindustrie untersucht [30] und mit Feldbauteilen verglichen. Abbildung 13 zeigt den zeitlichen Verlauf von Polarisationswiderständen verschiedener Verzinkungen im Testverlauf. Die Messungen erfolgten in der ersten Woche nach bestimmten Einzelzyklen des Tests und im Langzeitbereich nach 1, 2, 4 und 8 Wochen. Die einzelnen Verzinkungen liegen auf unterschiedlichen Leveln, ohne jedoch eine ausgeprägte Tendenz zur Erhöhung des Deckschichtwiderstands aufzuweisen. Die Passivierungen machen sich im Testverlauf stark bemerkbar, indem sie die Widerstände erhöhen und den Abfall auf niedrige Werte teilweise verzögern. Die normale Feuerverzinkung korrodiert in diesem Test am stärksten (geringste Widerstände), hat allerdings auch eine höhere Überzugsdicke und zeigt am Ende der Testzeit Rotrost und einen Einbruch des Polarisationswiderstandes. Die galvanisch abgeschiedenen Überzüge Zn-Fe und Zn-Ni weisen höhere Widerstände auf, jedoch ist die Korrosion trotzdem noch so stark (und die Überzugsdicke im Verhältnis geringer), dass sie im Testverlauf ebenfalls zum Rotrost und damit zum starken Einbruch der Widerstände führt. Für alle getesteten Verzinkungsvarianten ist in diesem Kurzzeitkorrosionstest keine Deckschichtbildung nachweisbar, wie sie unter atmosphärischen Bedingungen beobachtet wird. Dies liegt maßgeblich an den verschärften Prüfbedingungen (hohe Temperaturen, hohe Befeuchtungsdauern, starke Salzbelastung).
4.2.4 Abschätzung der Lebensdauer von verzinktem Stahl in der Freibewitterung
Wie gezeigt wurde, lassen sich die Methodik und die aus den Untersuchungen gewonnenen Kennwerte auf vielfältige Weise einsetzen und nutzen. Wissenschaftlich interessant sind Studien zur Bildung der Deckschichten unter Variation verschiedenster Parameter, wie z. B. der Auslagerungsbedingungen oder der Anwendungsbereiche, aber auch der Art der Zinküberzüge. Was viele Anwender jedoch auch interessiert ist, ob man aus diesen Kennwerten auf die zukünftige Lebensdauer einer Verzinkung im praktischen Einsatz schlussfolgern kann. Diese Fragestellung ist natürlich berechtigt und anhand der ermittelten Kennwerte ist dies auch prinzipiell möglich. Denn Polarisationswiderstände und Korrosionsstromdichten sind Kennwerte [31], aus denen bei Anwendung des Faraday'schen Gesetzes und der Materialkennwerte eine momentane Korrosionsgeschwindigkeit errechnet werden kann [32]. Die Frage bei der Interpretation eines so errechneten Wertes ist, ob dieser den zukünftigen „Normalzustand“ darstellt oder ob das System sich noch weiter verändert. Zur Abschätzung der Korrosionsrate bzw. Lebensdauer sind daher weitere Annahmen notwendig, und zwar
- dass die Deckschichtbildung abgeschlossen ist (stabile Phase, siehe Abb. 12) und
- dass sich die Medienbedingungen nicht mehr so stark verändern, dass ein erneuter Ab- und Wiederaufbau der Deckschicht erfolgt.
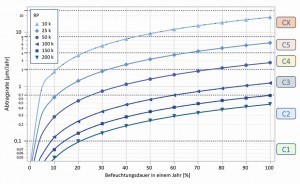 Abb. 14: Zusammenhang zwischen prognostizierter Abtragsrate für Zink bzw. verzinkten Stahl, der mittleren Befeuchtungsdauer und dem ermittelten Polarisationswiderstand (RP) Für immobile Objekte (Installationen im Bauwesen) sind die Medienbedingungen über ein Jahr betrachtet saisonal und standortbedingt zwar unterschiedlich, jedoch wiederkehrend relativ konstant und einfach zu bestimmen. Damit lässt sich zur Vereinfachung die mittlere Befeuchtungsdauer über ein Jahr ansetzen (die Korrosion im abgetrockneten Zustand ist vernachlässigbar) und damit die zukünftige Korrosionsgeschwindigkeit und eine Restlebensdauer für einen Zinküberzug errechnen. Wenn man diesen Ansatz verfolgt, erhält man Werte, die plausibel sind und im Bereich der normativen Abtragswerte für Zink in bestimmten Expositionsklassen liegen, vergleiche DIN EN ISO 9223 [33]. Abbildung 14 veranschaulicht den Zusammenhang zwischen prognostizierter Abtragsrate für Zink, der mittleren Befeuchtungsdauer und dem ermittelten Polarisationswiderstand. Durch gestrichelte Linien sind die Grenzbereiche C1 bis CX der Abtragsraten nach einem Jahr für Zink gekennzeichnet.
Abb. 14: Zusammenhang zwischen prognostizierter Abtragsrate für Zink bzw. verzinkten Stahl, der mittleren Befeuchtungsdauer und dem ermittelten Polarisationswiderstand (RP) Für immobile Objekte (Installationen im Bauwesen) sind die Medienbedingungen über ein Jahr betrachtet saisonal und standortbedingt zwar unterschiedlich, jedoch wiederkehrend relativ konstant und einfach zu bestimmen. Damit lässt sich zur Vereinfachung die mittlere Befeuchtungsdauer über ein Jahr ansetzen (die Korrosion im abgetrockneten Zustand ist vernachlässigbar) und damit die zukünftige Korrosionsgeschwindigkeit und eine Restlebensdauer für einen Zinküberzug errechnen. Wenn man diesen Ansatz verfolgt, erhält man Werte, die plausibel sind und im Bereich der normativen Abtragswerte für Zink in bestimmten Expositionsklassen liegen, vergleiche DIN EN ISO 9223 [33]. Abbildung 14 veranschaulicht den Zusammenhang zwischen prognostizierter Abtragsrate für Zink, der mittleren Befeuchtungsdauer und dem ermittelten Polarisationswiderstand. Durch gestrichelte Linien sind die Grenzbereiche C1 bis CX der Abtragsraten nach einem Jahr für Zink gekennzeichnet.
An zwei praktischen Beispielen soll der Zusammenhang verdeutlicht werden. Eine Probe eines verzinkten Stahls wurde unter Stadtbedingungen für ein Jahr frei bewittert. An der Probe wurde ein Polarisationswiderstand von durchschnittlich ca. 150 kΩcm2 ermittelt (vergleichbar mit Abb. 11, Messung mit Gel-Elektrolyt). Aus dem Polarisationswiderstand errechnet man die Korrosionsstromdichte und daraus, unter Berücksichtigung der Dichte und der Wertigkeit des Zinkions, die in Lösung gegangene Zinkmenge. Diese wird als Masseverlust pro Jahr und m2 angegeben, oder bei Annahme einer gleichmäßigen Metallauflösung als Abtragsrate in µm/Jahr. Da die Oberfläche nur eine bestimmte Zeit des Jahres befeuchtet ist, benötigt man noch die Dauer der Befeuchtung (τ), da Korrosion nur unter Vorhandensein von Wasser an der Oberfläche abläuft. Nach DIN EN ISO 9223 [33] werden Zeiten mit einer Temperatur > 0 °C und eine relative Luftfeuchte > 80 % als „befeuchtet“ definiert. Die mittlere Befeuchtungsdauer für den Standort wurde anhand von Wetterdaten des Deutschen Wetterdienstes (DWD) vom Autor ermittelt [34]. Die Rechnung mit 150 kΩcm2 und einer mittleren Befeuchtungsdauer von 34 % ergibt eine durchschnittliche Abtragsrate von ca. 0,24 µm/Jahr. Dieser Wert liegt genau im Bereich der Expositionsklasse C2, welche für Zink Werte von 0,1 bis 0,7 µm/Jahr im ersten Jahr der Auslagerung angibt. Da sich die Deckschicht der Probe nach einem Jahr bereits stabilisiert hat, ist solch ein niedriger Wert plausibel. Ein weiteres Beispiel betrifft einen maritimen Standort (Insel Helgoland). Auch hier wurden Proben für ein Jahr ausgelagert und der Deckschichtwiderstand mittels elektrochemischer Messungen mit einem Gel-Elektrolyten ermittelt. Aus einem mittleren Polarisationswiderstand von 50 kΩcm2 und einer durchschnittlichen Befeuchtungsdauer von 63 % errechnet sich eine durchschnittliche zukünftige Abtragsrate von ca. 1,74 µm/Jahr. Auch dieser Wert ist plausibel, unter Berücksichtigung stationärer Verhältnisse und der Expositionsklasse C3 (0,7 bis 2,1 µm/Jahr), wie sie heutzutage in bestimmten maritimen Bereichen Nordeuropas üblich ist. Ein Zinküberzug von 100 µm Dicke hätte unter diesen Bedingungen eine Lebensdauer von mehr als 50 Jahren, unter Annahme zukünftiger konstanter Bedingungen.
Natürlich lassen sich im Detail zu jedem individuellen Fall immer neue Besonderheiten finden, wie z. B. lokal veränderte Mikroklimate, werkstoffliche und konstruktive Unterschiede, Auswaschen von Zink durch Niederschläge, Abrieb u.v.a.m. Dies ist der Tatsache geschuldet, dass die Korrosion eine System-Eigenschaft mit vielen Einflussgrößen ist, die miteinander wechselwirken. Im Fall der Deckschichten vereinen sich jedoch die Einflussgrößen Material und Umgebungsbedingungen und führen dazu, dass die Schicht die Historie der korrosiven Belastung wie eine Art Fingerabdruck in sich trägt. Daher ist der Deckschichtwiderstand ein zuverlässiger Kennwert, aus dem sich bei Kenntnis weiterer Bedingungen nützliche Schlussfolgerungen ziehen lassen, wie z. B. die Abschätzung der Abtragsrate und daraus folgernd der Lebensdauer eines Zinküberzugs. Bezüglich des vorgestellten Rechenmodells kann man die Auffassung von George Box teilen, dass Modelle zwar alle falsch, aber einige eben doch nützlich sind. Die hier dargestellte Methodik und die daraus ableitbaren Erkenntnisse führen nach Ansicht des Autors weiter als alle bisherigen Prüfungen zur atmosphärischen Korrosion von verzinktem Stahl. Denn genau die vorher genannten Besonderheiten lassen sich mit der beschriebenen messtechnischen Herangehensweise viel einfacher bezüglich ihrer Auswirkungen erfassen und bewerten, auch unter praktischen Bedingungen.
5 Zusammenfassung
Gel-artige Elektrolyte haben in den letzten Jahren verstärkt Aufmerksamkeit und Anwendung im Bereich der Korrosionsuntersuchungen und -prüfungen erlangt. Mit ihrer Verwendung für die Korrosionsdiagnostik lassen sich viele neue Einsatzmöglichkeiten erschließen. Die elektrochemische Sensorik und die Handhabung können deutlich vereinfacht werden, was die Akzeptanz für den praktischen Einsatz erhöht. Darüber hinaus gelingt bei einer Reihe von oberflächentechnischen Maßnahmen im Korrosionsschutz deren messtechnische Charakterisierung, für die es bisher nur unbefriedigende Lösungen gab. Anwendungen wie das Korropad und Varianten davon sind bereits in einigen Branchen etabliert oder auf dem Weg dahin. Auch viele wissenschaftliche Fragestellungen lassen sich effektiver bearbeiten und führen schneller zu neuen Erkenntnissen.
Dass agar-basierte Gel-Elektrolyte hervorragend für die Korrosionsdiagnostik geeignet sind, liegt an ihren einzigartigen Eigenschaften. Bereits mit geringem Polymeranteil sind stabile Gele herstellbar, in denen der flüssige Elektrolyt durch das Gel-Netzwerk mit Porengrößen im Nanometerbereich immobilisiert wird. An der Oberfläche bzw. zwischen der Oberfläche und den Messelektroden bildet sich synäresebedingt ein dünner Elektrolytfilm, was elektrochemische Messungen ermöglicht. Das Gel-Netzwerk führt auch dazu, dass die Beweglichkeit von Teilchen einer gewissen Größe eingeschränkt wird. Dadurch steigt die Erkennbarkeit von lokalen Reaktionen, wenn über Farbindikationen die Ionespezies am Ort ihrer Entstehung komplexiert und festgesetzt werden. Weiterhin führen der dünne Elektrolytfilm und der gehemmte Stofftransport im Gel dazu, dass Korrosionsreaktionen gehemmt ablaufen und einfacher mit elektrochemischen Methoden analysiert werden können. Dies ermöglicht es, Schutzsysteme mit geringen Schichtgewichten nachzuweisen und zu quantifizieren, wie beispielsweise das Vorhandensein von VCI als temporäre Korrosionsschutzmaßnahme.
Die Verwendung von Gel-Elektrolyten zur Bestimmung von Deckschichtwiderständen an Zinküberzügen ist eine weitere aussichtsreiche Applikation, die zukünftig zu einem Normentwurf führen soll. Das Ziel besteht darin, die Handhabung der Methode zu vereinheitlichen und vergleichbarer zu machen. Die Weiterverarbeitung der elektrochemischen Kennwerte ermöglicht eine Abschätzung zukünftiger Abtragsraten von Zinküberzügen in der Freibewitterung. Die errechneten Werte geben das reale Verhalten bereits erstaunlich gut wieder. Der sensorische Aufwand dafür ist verhältnismäßig gering und dank der Fortschritte im Bereich mobiler elektrochemischer Messtechnik sind in Zukunft relativ einfache Messgeräte vorstellbar.
Danksagung:
Der Autor dankt Frau M.Sc. Christine Becker (OvGU Magdeburg) für die Durchführung der Messungen zum Elektrolytfilm, Herrn M.Sc. Ludwig Gropler (OvGU Magdeburg) für das 3D-Design und den Druck von Sensoren, der iLF Magdeburg GmbH für die Durchführung der rheologischen Messungen und der BAM Berlin (FB 7.6) für die chemische Analytik der Agar-Rohstoffe. Weiterhin gilt Dank der CORPAC Deutschland GmbH & Co. KG und der Mubea Fahrwerksfedern GmbH für die gute und produktive Zusammenarbeit. Besonderer Dank gilt auch Herrn M.Sc. Sebastian Hütter (OvGU) für das Programmieren der Bildauswertung.
Förderhinweis: Gefördert Deutsche Forschungsgemeinschaft (DFG) – Projektnummer 330472124.
Literatur
[1] Laque, F.L.; May, T.P.; Uhlig, H.H.: Corrosion in Action, International Nickel Company Canada, 1955
[2] Isaacs, H.S.; Adzic, G.; Jeffcoate, C.S.: Visualizing Corrosion, Corrosion 56 (2000) 10, 971–978, https://doi.org/10.5006/1.3294386
[3] DIN EN ISO 10309:2016-08: Metallische Überzüge – Prüfverfahren zur Bestimmung der Porosität – Ferroxylprüfung (ISO 10309:1994), Deutsche Fassung EN ISO 10309:2016
[4] Petersen, P.; Emnéus, H.: The Ferroxyle Test as a General Test of the Corrosiveness of Surgical Appliances Made from Stainless Steel or Co-Based Alloys of Stellite- Type, Mainly Vitallium and Neutrilium, Acta Orthopaedica Scandinavica, 29, 1-4, 1959, 331–340, https://doi.org/10.3109/17453675908988808
[5] Lehmann, J.; Burkert, A.; Müller, T.; Bohlmann, T.; Burkert, A.: Schlussbericht zu dem IGF-Vorhaben 17136 N/1 Detektion korrosionsempfindlicher Oberflächen nichtrostender Stähle durch die Verarbeiter, verfügbar auf researchgate.net
[6] Patentschrift DE 10 2010 037 775 B4: Auflage für den Nachweis von korrosionsempfindlichen Metalloberflächen und Verfahren zum Nachweis von korrosionsempfindlichen Metalloberflächen, Patent erteilt am 8.5.2014
[7] Rosemann, P.; Kauss, N.; Heyn, A.: KorroPad-Prüfung – Anwen[1] dungen aus Industrie und Forschung, 3-Länder-Korrosionstagung – Korrosion ist kein Zufall – Neue Messmethoden, Analytik und Simulation, Mai 2019, Frankfurt a. Main, verfügbar auf researchgate.net
[8] Rosemann, P.; Müller, T.; Babutzka, M.; Heyn, A.: Influence of microstructure and surface treatment on the corrosion resistance of martensitic stainless steels 1.4116, 1.4034, and 1.4021, Materials and Corrosion, 66, 2015, 45–53, https://doi.org/10.1002/maco.201307276
[9] Reinemann, S.; Babutzka, M.; Rosemann, P.; Lehmann, J.; Burkert, A.: Influence of grinding parameters on the corrosion behavior of austenitic stainless steel, Materials and Corrosion, 70, 2019, 1776–1787, https://doi.org/10.1002/maco.201910874
[10] Kauss, N.; Heyn, A.; Halle, T.; Rosemann, P.: Detection of sensitisation on aged lean duplex stainless steel with different electrochemical methods, Electrochimica Acta 317 (2019) 17–24, https://doi.org/10.1016/j.electacta.2019.05.081
[11] Newton, C.J.; Sykes, J.M.: A galvanostatic pulse technique for investigation of steel corrosion in concrete, Corrosion Science, 28, Nr. 11, 1988, 1051–1074, https://doi.org/10.1016/0010-938X(88)90101-1
[12] Spark, A.J.; Cole, I.; Law, D.; Ward, L.: The effect of peptide based nutrients on the corrosion of carbon steel in an agar based system, Corrosion Science 110, 2016, 174–181, https://doi.org/10.1021/acs.est.7b00437
[13] Spark, A. J.; Cole, I.; Law, D.; Marney, D. and Ward, L.: Investigation of agar as a soil analogue for corrosion studies. Materials and Corrosion 67 (2016), S 7–12, https://doi.org/10.1002/maco.201508312
[14] Spark, A.J.; Law, D.W.; Ward, L.P.; Cole, I.S.; Best, A.S.: Effect of Pseudomonas fluorescens on Buried Steel Pipeline Corrosion, Environmental Science & Technology, 51 (15), 2017, 8501–8509, https://doi.org/10.1021/acs.est.7b00437
[15] Vanbrabant, J.; van de Velde, N.: Industrial application of an electrochemical corrosion test using a gel matrix as simulation for atmospheric and solid media, Proceedings: European General Galvanizers Association Intergalva Berlin, Vol. 19, June 7th, 2000, 29/1 to 29/13
[16] Shao, X.M.; Feldman, J.L.: Micro-agar salt bridge in patch-clamp electrode holder stabilizes electrode potentials, Journal of Neuroscience Methods 159, 2007, 108–115, https://doi.org/10.1016/j.jneumeth.2006.07.001
[17] Monrrabal, G.; Guzmán, S.; Hamilton, I.E.; Bautista, A.F.; Velasco, F.: Design of gel electrolytes for electrochemical studies on metal surfaces with complex geometry, Electrochimica Acta, Volume 220, December 2016, 20–28, http://dx.doi.org/10.1016/j.electacta.2016.10.081
[18] Monrrabal, G.; Ramírez-Barat, B.; Bautista, A.; Velasco, F.; Cano, E.: Non-Destructive Electrochemical Testing for Stainless-Steel Components with Complex Geometry Using Innovative Gel Electrolytes. Metals,8, 2018, 500, https://doi.org/10.3390/met8070500
[19] Monrrabal, G.; Huet, F.; Bautista, A.: Electrochemical noise measurements on stainless steel using a gelled electrolyte, Corrosion Science, Volume 148, March 2019, Pages 48–56, https://doi.org/10.1016/j.corsci.2018.12.004
[20] Monrrabal, G.; Bautista, A.; Valesco F.: Use of Innovative Gel Electrolytes for Electrochemical Corrosion Measurements on Carbon and Galvanized Steel Surfaces, CORROSION, Vol. 75, No. 12, December 2019, 1502–1512, https://doi.org/10.5006/3309
[21] Cano, E.; Crespo, A.; Lafuente, D.; Ramirez Barat, B.: A novel gel polymer electrolyte cell for in-situ application of corrosion electrochemical techniques, Electrochemistry Communications, 41 (2014), 16–19, https://doi.org/10.1016/j.elecom.2014.01.016
[22] Di Turo, F.; De Vito, C.; Coletti, F.; Mazzei, F.; Antiochia, R.; Favero, G.: A multi-analytical approach for the validation of a jellified electrolyte: Application to the study of ancient bronze patina, Microchemical Journal, Vol. 134, 2017, 154–163, https://doi.org/10.1016/j.microc.2017.05.015
[23] Babutzka, M.; Burkert, A.; Heyn, A.: Korrosionsuntersuchungen mit gelartigen Elektrolyten zur Beschreibung der Korrosionsschutzwirkung von Zinküberzügen, 16. Sommerkurs Werkstoffe und Fügen: Magdeburg, 8. und 9. September 2017, 119–128, http://dx.doi.org/10.25673/5002
[24] Babutzka, M.; Heyn, A.: Dynamic tafel factor adaption for the evaluation of instantaneous corrosion rates on zinc by using gel-type electrolytes, IOP Conf. Ser.: Mater. Sci. Eng. 181, 2017, 012021, https://doi.org/10.1088/1757-899X/181/1/012021
[25] Labille, J.; Fatin-Rouge, N.; Buffle, J.: Local and Average Diffusion of Nanosolutes in Agarose Gel: The Effect of the Gel/Solution Interface Structure, Langmuir, 23, 2007, 2083–2090, https://doi.org/10.1021/la0611155
[26] Vaucher, S.; Li, M.; Mann, S.: Synthesis of Prussian Blue Nanoparticles and Nanocrystal Superlattices in Reverse Microemulsions, Angew. Chem. Int. Ed., 39, 1793–1796 http://www.doi.org/10.1002/(SICI)1521-3773(20000515)39:10<1793::AID-ANIE1793>3.0.CO;2-Y
[27] Ogston, A.G.; Preston, B.N.; Wells, J.D.: On the transport of compact particles through solutions of chain polymers, Proc. R. Soc. London, A. 1973333, 1973, 297–316, https://doi.org/10.1098/rspa.1973.0064
[28] Somma, M.; Querci M.: The Analysis of Food Samples for the Presence of Genetically Modified Organisms, Session 5: Agarose Gel Electrophoresis, 62, https://doi.org/10.2760/5277
[29] Normentwurf für ein Prüfverfahren zur Bestimmung von Deckschichtwiderständen an Zinküberzügen mittels Gel-artiger Elektrolyte – GELELEK, Forschungsvorhaben in der Forschungsinitiative des BMWi WIPANO, Projektträger Jülich, Berlin
[30] Killik, A.: Einflussfaktoren auf die Korrosion von unterschiedlich verzinkten Stahlprüfkörpern in Kurzzeitkorrosionstests und im Feld, Dissertation, Otto-von-Guericke-Universität Magdeburg, 2016
[31] J.R. Scully: Polarization Resistance Method for Determination of Instantaneous Corrosion Rates, Corrosion Vol. 56, Nr. 2, 2000, 199–218, NACE International, https://doi.org/10.5006/1.3280536
[32] ASTM G3−14: Standard Practice for Conventions Applicable to Electrochemical Measurements in Corrosion Testing, Reapproved 2019
[33] DIN EN ISO 9223:2012: Korrosion von Metallen und Legierungen – Korrosivität von Atmosphären – Klassifizierung, Bestimmung und Abschätzung
[34] Heyn A.: Bewertung der Korrosivität von Atmosphären anhand von Wetterdaten, 16. Sommerkurs Werkstoffe und Fügen: Magdeburg, 8. und 9. September 2017, 129–138, http://dx.doi.org/10.25673/5002













