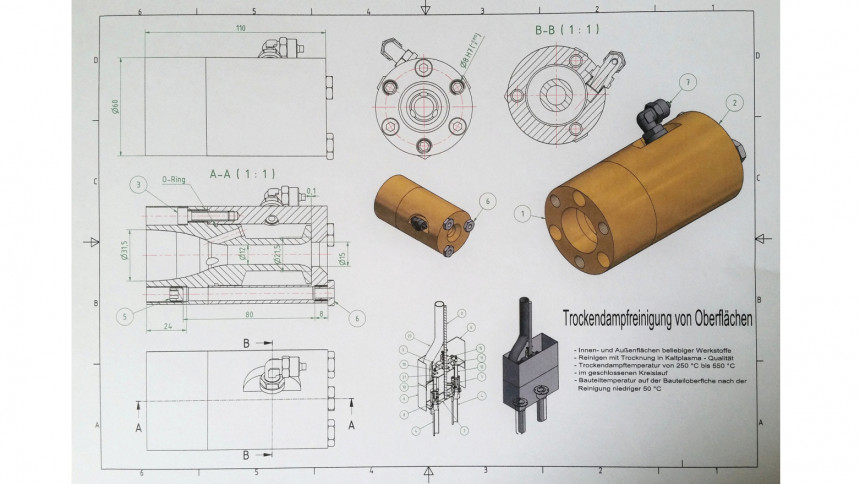
Hindernisse und Hemmnisse bisheriger Reinigungstechnologien der nass-chemischen Oberflächenreinigung
Auf der Oberfläche eines Bauteiles wird zeitlich und räumlich definierte Reinheit erhalten. Dies ist immer ein durch Menschen und seinen Automaten gesteuerter aktiver Prozess, der in der Zeit und in dem jeweiligen Raum begrenzt erhalten werden kann. Die gegenwärtig in der Serienfertigung angewendeten Reinigungstechnologien sind Verfahren auf nass-chemischer Grundlage. Wasserlösliche Reiniger von pH-Wert „sauer“ bis „stark basisch“ finden Anwendung. Die häufigsten Anwendungen arbeiten im pH-Wert – Bereich 7 bis 9. Je nach Werkstoff werden die chemischen Zusätze im Reiniger ausgewählt. Als Abschluss der Reinigung verbleibt ein Passivierungsfilm, der die von Fremdstoffen gereinigte Bauteiloberfläche gegen undefinierte Verschmutzung versiegelt. Korrosion oder auch Reduktionvorgänge werden verhindert oder minimiert. In jedem Fall der Reinigung bilden sich chemisch bedenkliche Rückstände, die einer besonderen Aufbereitung in der Entsorgung bedürfen. Das Wasser als Lösungsmittel wird in sehr hoher Menge in diesen Prozessen eingesetzt und erfordert somit Beschaffungsaufwand und Kostenaufwand in enormer Höhe. Die Bauteilereinigung ist kostenintensiv und erfordert pro Bauteil vergleichbare Energieaufwendungen wie in der spanenden Bearbeitung. Jeder Typ von Bauteil erfordert seine Reinigungstechnologie. Zeit- und Kostenaufwand der bisherigen Reinigungstechnologien wachsen, da die Anforderungen an die Ergebnisse der Reinigung, die verbleibenden Fremdstoffe auf der Bauteiloberfläche in Menge und in Größe geringer werden müssen. Die Bauteileigenschaften in den Bereichen der Automatisationen und in den Bereichen moderner Maschinen und Anlagen fordern dies.
Die bauteilgebundenen Technologien der Reinigungschemie behindern die multiple Nutzung der Reinigungsanlagen. Der meist offene Energiekreislauf verursacht expandierende Kosten. Geschlossene Energiekreisläufe mit geringer Energieabgabe an die Umgebung sind die bisherige Ausnahme. Die automatische Überwachung der chemischen Konzentrationen in der Reinigungslösung, bestehend aus Wasser, Reiniger, Kühlschmiermitteln, Spänen, Schmutzpartikel aller Art usw. ist bisher unzureichend gelöst. Nur die manuelle, personengebundene Laboranalyse ergibt auswertbare Ergebnisse. Die automatisierten Messtechniken sind vergleichende Messungen, mehr oder weniger vom Bedienpersonal abhängig auswertbar. Es werden meist vergleichende Steuerungen genutzt.
|
Hindernisse und Hemmnisse |
Auswege und Umwege bisheriger Reinigungstechnologien |
|
Material des Bauteils – abhängige Zugabe chemischer Reinigungskonzentrate |
Die Dosierung mit Konzentrationsüberwachung, meist Leitwertmessungen oder die proportionale Zugabe bezogen auf den Frischwasserverbrauch, Partikelzähler, Tintentests, Wasserbruch- Ablauftest, pH-Wert-Über- wachung, Wasserhärteprüfung, regelmäßige Titrationen im Labor, von Hand Nachdosierungen oder die Korrekturen der Konzentrationen, aufwendige Aufbereitung der Medien |
|
Art der Verschmutzung wird mit einer Art Breitband-Lösung bearbeitet |
Unterschiedliche chemische Zusätze von sauer bis basisch, mechanische Vorreinigungen wie Ultraschall oder Bürsten, Dauer der Reinigung, Einwirkzeiten verlängern, Hochdruckwasserstrahlen |
|
Mediendosierung, Medienverbrauch |
Den Wasserverbrauch durch die Verdunstung und die Verschleppung erzeugen, um den Zulauf von Frisch- wasser zur Verdünnung der Reinigerlösung zu erreichen, das Abscheiden von gelösten Fremdpartikel durch Filtrationen, die Baderwärmung und somit die Bauteiler- wärmung, um die höhere Lösungsbereitschaft von warmem Wasser zu nutzen und die Trocknung der Bauteile zu ermöglichen, hoher Energieeinsatz, da meist offene Energieketten, Reinigernachdosierung |
|
Bauteilspezifische Reinigungstechnologie und spezielle Reinigungsanlage |
Die Schaffung eines Baukastensystems der Reinigungsanlagentechnik, der Wechsel der „Werkzeuge“ und Medien abhängig vom Bauteil |
|
Steuerung anfällig, mit großer Toleranz, Bediener überwacht |
Fachpersonal, die Kontrolle nach Prüfplan der Parameter, die begrenzte Mehrmaschinenbedienung, die Grenzwerte großzügig vorgegeben, die geringe Anzahl von Stich- proben in Laborqualität, der Vorbeugende Wasser- wechsel und die Überdimensionierung der Anlagen- aggregate wie Pumpen, Heizung und Gebläse |
Die Hemmnisse der Praxis, wie stark schwankende chemisch-physikalische Parameter der Reinigerlösung, unzureichende Messtechnik, fehlendes oder zu wenig Fachpersonal, Stichproben-Kontrolle der Reinigungsergebnisse mit Laufzeiten von 4 bis 10 Stunden pro Stichprobe, spezielle Auswertetechnik und Auswerteräumlichkeiten in Laborqualität, lassen nur bedingte reproduzierbare Ergebnisse der Reinigungsprozesse zu, siehe Tabelle 1. Die anzustrebende stündliche Kontrolle der Reinigungslösungen, Wasch- und Spüllösungen, wird wegen des Zeit- und Materialaufwandes kaum ausgeführt. Die Toleranzbreite der Reinigungsergebnisse des Prozesses erfordert mehr spezielle Aufwendungen. Die Vielzahl der zu steuernden Parameter erschwert den Erhalt der gleichbleibenden Qualität des Produktionsprozesses.
Die Definition von Reinheit
Bisher ist die direkte Messung nur als definierte Stichprobe möglich. Auf der Bauteiloberfläche werden definierte Teilflächen durch das Mikroskop betrachtet und die Fremdpartikel werden vermessen und gezählt. Alternativ werden Bauteilflächen definiert mittels Reinigerlösung abgereinigt, das abfließende Medium wird über einen Prüffilter gegossen, um dann anhand der vorgegebenen Grenzwerte das Ergebnis zu bewerten. Absolute Reinheit ist eine theoretische Größe. Die eingesetzten Messmittel zur Bestimmung der Fremdpartikel geben den Wert vor. Aus der Konstruktion und aus der Technologie des Bauteils wird ein prüfbarer, reproduzierbarer Wert festgelegt.
Es werden Aussagen zu den Fremdpartikeln vorgegeben. Das Umfeld der Bauteile wirkt direkt auf den Zustand der Verschmutzung. Soll die Sauberkeit der Oberfläche einen Wert an Fremdpartikeln nicht überschreiten, muss die Umgebung der Bauteile um das 10-fache „sauberer“ sein, d.h. alle Parameter dürfen nur maximal 1/10 der Werte der Fremdpartikel haben. In der Praxis werden Partikel kleiner 100 µm Länge gezählt, um auch die Möglichkeit der Verklumpung zu erfassen. Die Partikel werden klassiert.
Die gereinigte Bauteiloberfläche ist dem Sauerstoff ausgesetzt, d.h. die Oberfläche wird oxidieren. Dieser Vorgang kann durch Auftragen eines Passivierungsfilms verhindert oder verzögert werden. Dieser Passivierungsfilm ist als Ergebnis der Reinigung immer auf der Bauteiloberfläche. Das „reine“ Bauteil ist definiert unrein.
Wird also über Reinheit gesprochen, muss stets die Frage der Definition messbar, reproduzierbar mit einer quantifizierten Aussage beantwortet werden.
Ziel ist das Entfernen von Fremdpartikel aus metallischem Werkstoff von der Bauteiloberfläche. Die Größe der Partikel liegt zwischen 50 µm < Länge < 1000 µm fester Partikel, zwischen 10 µm< Breite < 1000 µm fester Partikel bei Materialdicke von größer 10 µm. In der Ausdehnung größere Partikel sind meist Klemmspäne, die nicht oder nicht reproduzierbar entfernt werden können.
Fasern bis 5 mm Länge werden von der Bauteiloberfläche entfernt. Faserknäuel ab einer bestimmten Größe und Masse werden unregelmäßig entfernt.
Die Regeln nach VDA 19 und die Regeln nach ISO 16 232 /01…10 werden als Grundlage für die Prüfungen und Auswertungen von Reinheit der Bauteiloberflächen genutzt.
Die Trennung physikalischer Bindungen
Es sind nicht „Haken und Ösen“, die eine Verbindung ausmachen. Nicht mechanische, formschlüssige Verbindungen verbinden Fremdpartikel mit einer Bauteiloberfläche. Es sind die Eigenschaften der Atome und Elektronen, der freien Ionen und deren Wechselwirkungen zueinander. Hier bilden sich abhängig von den Parametern der Partikel Anziehungskräfte aus.
Die Trennung von Fremdpartikel, die Aufhebung der Haftung, bedeutet die Entladung der Verbindung, die Aufhebung der Anziehungskräfte mit anschließendem mechanisch verursachten Transport von Fremdpartikeln.
Die elektrische Oberflächenentladung kann auf drei Wegen erfolgen. Das Grundmaterial und die Art der Erdung beeinflussen wesentlich die Schnelligkeit der Oberflächenentladung. Gut elektrisch leitende Werkstoffe und geringer Übergangswiderstand zur Erdung sind bei metallischen Werkstoffen in der Regel gegeben. Die Schichtung der bearbeiteten Schichten nach der Bearbeitung bildet zum Grundwerkstoff einen Übergangswiderstand, ja eine Form der Isolation der äußeren Ladung zum leitenden Grundwerkstoff. Die Umgebungsstrahlung und die umgebenden Medien, gasförmig oder flüssig, tragen mit ihrer elektrischen Ladung zur Oberflächenentladung des Körpers bei.
Quantifizierung der Bindungsenergie zwischen Objektoberfläche und Fremdpartikeln
Die OH-Gruppen können als O- und OH-Gruppen vorliegen, also negativ geladen oder neutral sein. Da sich ein chemisches Gleichgewicht einstellen wird, ist die Konzentration der O- (d.h. die Oberflächenladung) eine Funktion der Konzentration der H+ in der Lösung (also des pH-Wertes). Je höher die H+-Konzentration, umso niedriger der pH-Wert, um so weniger O--Gruppen sind vorhanden.
Modellvorstellung
Entgegengesetzt geladene Ionen ziehen sich an, gleichnamig geladene Ionen stoßen sich ab. Aus diesen Gründen sind Ionen in einer Lösung nicht willkürlich verteilt, sondern besitzen eine gewisse Nahordnung, in der Anionen eher in der Nähe von Kationen zu finden sind und umgekehrt. Elektroneutralität der Lösung ist dabei gewahrt. Im Gegensatz zum Ionengitter können sich Ionen in Lösung nicht vollständig regelmäßig anordnen, weil Lösungsmittelmoleküle als Dielektrikum die Coulombschen Wechselwirkungen abschwächen, worauf die thermische Bewegung zu einer stärkeren Verteilung der Ionen führt. Im zeitlichen Mittel befindet sich aber jedes Ion im Zentrum einer Wolke aus entgegengesetzt geladenen Ionen (in Abbildung 1 durch Kreise angedeutet). Diese Ionenwolken schirmen die Ladung des Zentralions ab, was der Grund für die Einführung der Aktivität als „wirksame Konzentration“ bei Ionen ist [1].
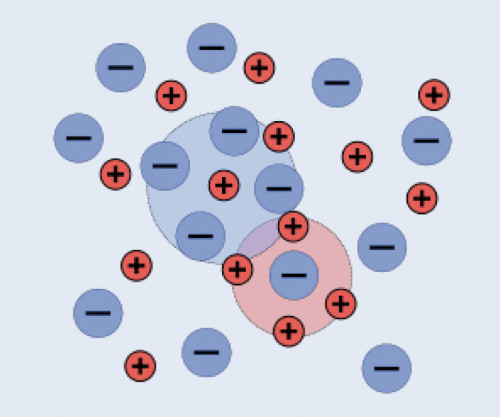 Abbildung 1: Ionenverteilung in einer Lösung
Abbildung 1: Ionenverteilung in einer Lösung
„Ausgehend von diesen Modellvorstellungen haben P. Debye und E. Hückel durch Kombination der Poisson-Gleichung mit der Boltzmann-Statistik zur Beschreibung der Ionenverteilung einige in der Elektrochemie häufig benutzte Gleichungen abgeleitet. Zur Vereinfachung benutzten sie dabei die folgenden Größen
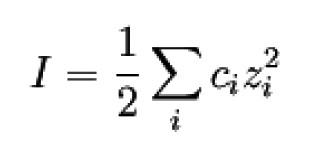
Ionenstärke I
ci Konzentrationen der Ionensorten in der Lösung
zi Ladungszahlen der Ionensorten
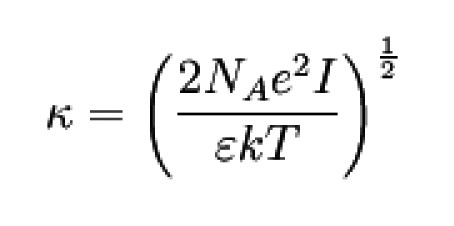
e Elementarladung
ε Permittivität des Lösungsmittels;
k Boltzmannkonstante (s. Physikalische Konstanten)
T Temperatur
NA Avogadro-Konstante
Aktivitätskoeffizient f der Ionensorte i
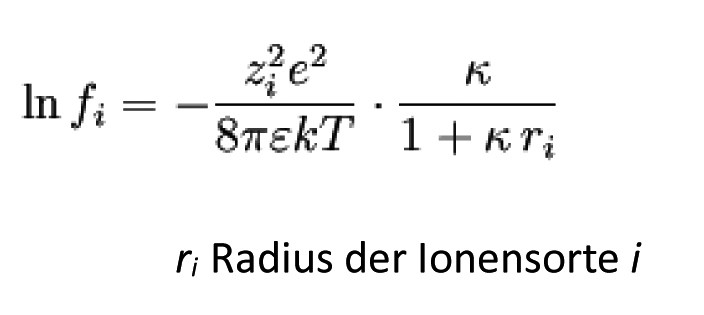
Diese Gleichung wird oft als erweitertes
Debye-Hückel-Grenzgesetz in der Form
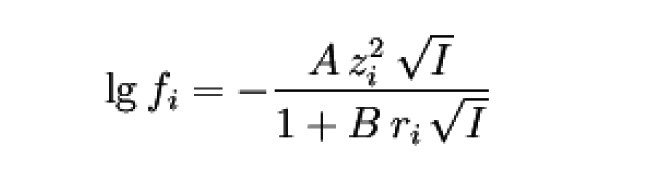
verwendet. Darin sind
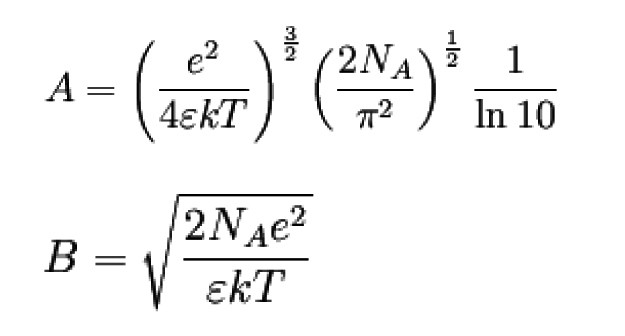
Der Gültigkeitsbereich liegt ca. bei mol dm–3.
Radius der Ionenwolke
Es stellte sich heraus, dass sich das Inverse von κ als Radius der Ionenwolke interpretieren lässt.
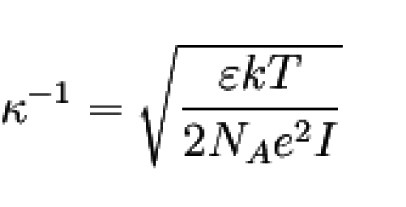
Diesen Radius nennt man auch Abschirmlänge oder
Debye-Länge.
Debye-Hückel-Grenzgesetz

Darin ist A = 0.509 dm3/2 mol–1/2 zu setzen, wenn Wasser bei 25 °C als Lösungsmittel verwendet wird. Für andere Temperaturen und/oder Lösungsmittel muss es nach der oben angegebenen Gleichung berechnet werden.
Das ist die für praktische Belange am häufigsten zitierte Gleichung, die sich in der Näherung ergibt. Sie gilt also für Ionenwolken, die wesentlich größer sind als das umschlossene Ion. In der Regel sind das sehr verdünnte Lösungen mit mol dm–3.
Mittlerer Aktivitätskoeffizient und Debye-Hückel-Grenzgesetz
Individuelle Aktivitätskoeffizienten (bzw. -aktivitäten) können zwar berechnet, aber aufgrund der Elektroneutralitätsbedingung nicht gemessen werden. Für den messbaren mittleren Aktivitätskoeffizienten eines Elektrolyten gilt
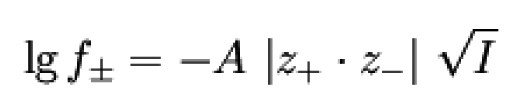
Literatur hierzu in [2][3].
Debye-Hückel-Onsager Theorie
Eine Verfeinerung des Modells von Debye und Hückel ist das Modell nach Debye-Hückel-Onsager. In diesem Modell wird zusätzlich die Hydrodynamik berücksichtigt. Dadurch wird das Modell leider mathematisch komplizierter. Eine ausführliche Herleitung würde im Rahmen dieser Lerneinheit zu weit führen, weshalb das Modell nur kurz vorgestellt wird.
Beim Anlegen eines äußeren Feldes wandern Zentralion und Ionenwolke in entgegengesetzter Richtung. Die Ionenwolke muss stets neu aufgebaut werden. Es entsteht ein Relaxationseffekt, d.h. es wird zusätzliche Reibung verursacht. Außerdem werden die Ladungsschwerpunkte von Zentralion und Ionenwolke verschoben (elektrophoretischer Effekt). Diese zusätzliche Bremswirkung muss zur Stokes'schen Reibung addiert werden. Als Endgleichung ergibt sich:
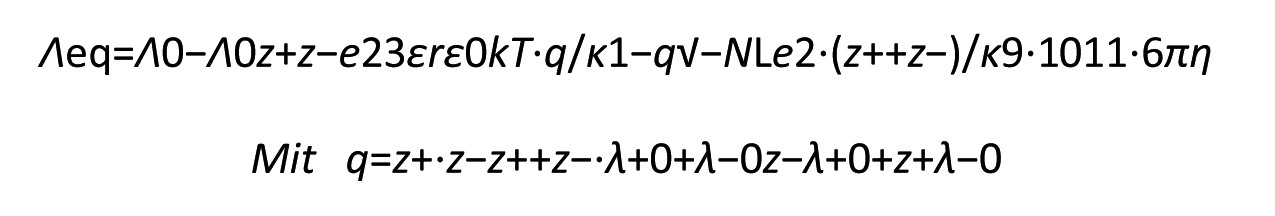
Für starke (1:1)-Elektrolyte vereinfacht sich die Gleichung zu:
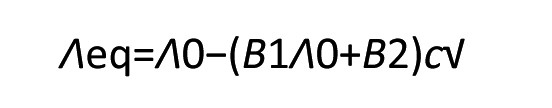
Diese Gleichung stimmt mit dem empirisch gefundenen Kohlrausch'schen Quadratwurzelgesetz überein. Eine detailierte Analyse der mikroskopischen Zusammenhänge zur Leitfähigkeit ist insbesondere bei frequenzabhängigen Untersuchungen (Impedanzmessung) notwendig [4].
Im Gegensatz zu elektrostatischen Kräften des täglichen Lebens, die über große Distanzen wirken können (z. B. Blitze), ist die Reichweite der elektrostatischen Kräfte in den untersuchten Systemen sehr klein. Die Ursache ist die Abschirmung von Ladungen durch Gegenionen aus der umgebenden Lösung, beschrieben durch die Debye-Hückl Theorie.
Das Messen von Oberflächenladungen ist nicht besonders einfach und es bedarf vor allem in ionischen Lösungen einiger Tricks. An Luft können physikalische Methoden verwendet werden, etwa die Kraft auf eine vibrierende geladene Platte in der Nähe der zu untersuchenden Oberfläche (Kraft im Plattenkondensator). Ist die Oberfläche elektrisch leitend, könnte direkt ein Voltmeter angeschlossen werden, jedoch sind viele für die Maschinenbauer interessanten Oberflächen elektrische Isolatoren. Daher werden andere Techniken benötigt. Einige der wenigen universell einsetzbaren Methoden sind Strömungspotential Messungen und Methoden, die direkt Kräfte messen, wie das Kraftmikroskop oder der SFA (surface force apparatus). In dieser Arbeit wurden keine Kraftmessungen mittels Kraftmikroskop ausgeführt. Diverse Messreihen aus der Literatur wurden gelesen und die von mir bewerteten Ergebnisse für die Zielstellung dieser Arbeit genutzt.
Polarität und Wasserlöslichkeit – Emulsionen und deren Strukturen in Kühlschmiermitteln
Als Emulsionen bezeichnen wir mindestens zwei nicht miteinander mischbare Flüssigkeiten. Eine Flüssigkeit überwiegt in der Menge und die anderen sind meist fein in der erstgenannten Flüssigkeit verteilt, nicht gelöst. Die Flüssigkeiten werden mechanisch zu einander bewegt, gerührt. Ruht die Bewegung, entmischen sich die Bestandteile der Emulsion. Durch Zugabe eines Emulgators kann die Entmischung verzögert werden, vollständiges Entmischen in ruhenden Flüssigkeiten kann jedoch nicht verhindert werden.
Bei Wasser in Öl-Emulsionen ist die Ölphase durchgängig, die Wasserphase ist in kleinen Tröpfchen darin verteilt (Beispiel: Streichfette). Der Wassergehalt von Wasser in Öl-Emulsionen darf höchstens 74 % betragen. Bei Öl in Wasser - Emulsionen sind die Verhältnisse umgekehrt: Die Wasserphase ist durchgängig, die Ölphase ist in kleinen Tröpfchen darin verteilt (Beispiel: Kühlschmiermittel). Eine Öl in Wasser-Emulsion muss mindestens 26 % Wasser enthalten. Befindet sich mehr als 6 Vol % Öl in Wasser gelöst, beginnt die Bildung einer Ölschicht auf der Flüssigkeitsoberfläche. Der Emulgator als Hilfsmittel zur stabilen Verteilung verschiedener Flüssigkeiten sind Tenside. Die Tenside können aus einem hydrophilen (wasserfreundlich) und/oder aus einem hydrophoben (lipophil, fettfreundlich) Teil zusammengesetzt sein.
Der hydrophile Teil lagert sich an der Grenzfläche zwischen Öl und Wasser am Wasser an, während der hydrophobe Teil im Öl (Fett) steckt. Man unterscheidet Öl-in-Wasser-(O/W-) und Wasser-in-Öl- (W/O-)Emulgatoren. Der Emulsionstyp (O/W bzw. W/O) wird nicht durch den Wasseranteil der Emulsion bestimmt, sondern durch den verwendeten Emulgator. Emulgatoren, bei denen die wasserfreundlichen Gruppen überwiegen, führen zu Öl-in-Wasser-Emulsionen. Überwiegen dagegen die fettfreundlichen Gruppen, so entstehen Wasser-in-Öl-Emulsionen [5].
Stoffe, die aus Ionen oder Molekülen, die Ladungen enthalten, bestehen, nennt man polar. Moleküle ohne diese Ladungen werden als nicht polar bezeichnet. Das Wassermolekül ist polar, da seine beiden Wasserstoffmoleküle eine positive Teilladung und sein Sauerstoffmolekül eine negative Teilladung besitzt. Da sich Gleiches in Gleichem löst, sind polare Stoffe (z. B. Salze) in Wasser besser löslich als nicht polare Stoffe, wie etwa Öl [6]. Kühlschmiermittel aus den Zerspanungsprozessen werden mit dem in dieser Arbeit gefundenem Verfahren von der Bauteiloberfläche entfernt.
Literatur
[1] https://de.wikipedia.org/wiki/Debye-H%C3%BCckel-Theorie
[2] Berson, J. A.: Chemical Creativity - Ideas from the Work of Woodward, Hückel, Meerwein, and Others, Wiley-VCH, Weinheim 1999
[3] www.chemie.de/lexikon/Debye-H%C3%BCckel-Theorie.html
[4] www.chemgapedia.de/vsengine/vlu/vsc/de/ch/13/vlu/echemie/leitfaehigkeit/leitfaehigkeit.vlu/Page/vsc/de/ch/13/pc/echemie/leitfaehigkeit/onsager.vscml.html
[5] www.chemie-master.de
[6] www.lenntech.de/element-und-wasser/loeslichkeit.htm#ixzz2riD7KbzY)