Aufgrund der emittierenden Alpha-Strahlung hat sich die eingehendere Risiko-Betrachtung in den meisten Fällen gegen den weiteren Einsatz dieses Elements und seiner chemischen Verbindungen entschieden. Dabei geht Thorium mit den bereits mehrere Jahre in der Entwicklung befindlichen Salzschmelz-Reaktoren für die gebändigte atomare Energie-Gewinnung einer hoffnungsvollen Zukunft entgegen. Und vielleicht ermöglichen moderne sicherheitstechnische Vorkehrungen auch noch weitere Anwendungen dieses reichlich vorhandenen Elements.
Die Entdeckungs-Geschichte des Thoriums
Schon 1815 besaß Berzelius eine Gesteinsprobe, in der er ein neues Mineral vermutete. Er ordnete dieses Mineral einem neuen Oxid zu und nannte schon das dazugehörige Metall nach dem germanischen Gott Thor. 1824 stellte sich jedoch heraus, dass es sich bei diesem vermeintlich neuen Mineral um Yttriumphosphat, YPO4, handelte [1].
Im Jahr 1898 entdeckten Marie Curie (1867–1934) und der deutsche Chemiker Gerhard Schmidt (1865–1949) zeitgleich die Radioaktivität von Thorium [2, 3], wobei die Veröffentlichung von Gerhard Schmidt zuerst erschien [4].
Aber erst 1914 gelang D. Lely, Jr. und L. Hamburger erstmals die Darstellung des reinen Thorium-Metalls nach dem Verfahren von dem niederländischen Chemiker Anton Eduard van Arkel (1893–1976) und dem niederländischen Physiker Jan Hendrik De Boer (1899–1971) [5, 6].
Thoriummetall und seine Eigenschaften
Das nach dem germanischen Gott Thor benannte Thoriummit dem Elementsymbol Th und der Ordnungszahl 90 steht im Periodensystem der Elemente in der Gruppe der Actinoide, umgeben von den Seltenerd-Metallen Lanthan (La), Cer (Ce) und Praseodym (Pr) sowie als Nachbarn von Actinium (Ac) und Protactinium (Pa) (Abb. 1). Mit seinem hohen Atomgewicht von 232,03 Dalton emittiert das Thorium Alpha-Strahlung mit einer Halbwertszeit von 1,405 · 1010 Jahren.
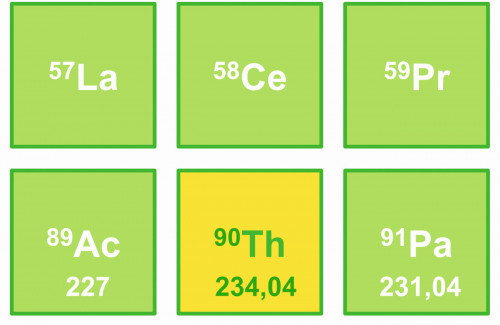 Abb. 1: Thorium und seine Nachbarn im Periodensystem der Elemente
Abb. 1: Thorium und seine Nachbarn im Periodensystem der Elemente
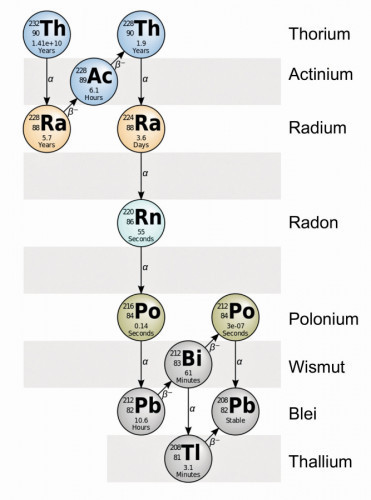 Abb. 2: 232Th-Zerfallsreihe (Quelle: https://en.wikipedia.org/wiki/Thorium)Der Thorium-Kern besteht daher aus 90 Protonen und 142 Neutronen, die 90 Elektronen in der Konfiguration [He] 6d2 7d2 auf verschiedenen Energieniveaus umkreisen.
Abb. 2: 232Th-Zerfallsreihe (Quelle: https://en.wikipedia.org/wiki/Thorium)Der Thorium-Kern besteht daher aus 90 Protonen und 142 Neutronen, die 90 Elektronen in der Konfiguration [He] 6d2 7d2 auf verschiedenen Energieniveaus umkreisen.
Mit dem Element Thorium beginnt eine lange Zerfallsreihe, die mit dem nicht radioaktiven Element Blei endet (Abb. 2).
Reines Thorium ist ein silberweißes Metall, das an der Luft bei Raumtemperatur stabil ist und seinen Glanz einige Monate behält. An der Oberfläche oxidiertes Metall, läuft langsam an der Luft an und wird grau und schließlich schwarz.
Die physikalischen Eigenschaften von Thorium hängen stark von seiner Reinheit ab. Viele raffinierte Thorium-Metalle enthalten Spuren von einigen Promille Thorium(IV)-dioxid, ThO2. Aber auch hochreines Thorium kann hergestellt werden. Es ist weich, sehr dehnbar und es lässt sich kalt walzen und ziehen.
Thorium ist polymorph mit zwei bekannten Modifikationen. Bei über 1400 °C wandelt es sich von einer kubisch-flächenzentrierten in eine kubisch-raumzentrierte Struktur um.
Von Wasser wird Thorium nur sehr langsam angegriffen, es löst sich aber auch in den meisten verdünnten Mineralsäuren, wie Flusssäure, Salpetersäure oder Schwefelsäure sowie konzentrierten Salz- und Phosphorsäuren nur langsam. Rot rauchende Salpetersäure, ein Gemisch aus 84 % Salpetersäure, HNO3, 13 % Distickstofftetroxid, N2O4, und 3 % Wasser sowie „Königswasser“, ein Gemisch aus drei Teilen konzentrierter Salzsäure und einem Teil konzentrierter Salpetersäure jedoch bringen Thorium-Metall gut in Lösung.
Pulverförmiges Thorium wirkt bei feiner Verteilung pyrophor, d. h. es verbrennt an der Luft mit weißer, hell leuchtender Flamme. Weitere Eigenschaften des Elements sind der Abbildung 3 zu entnehmen.
Thorium-Vorkommen und Preise
In der Erdkruste kommt Thorium mit einer Häufigkeit von 7 bis 13mg pro kg vor; damit ist es doppelt bis dreimal häufiger als Uran zu finden. Generell ist das Element aufgrund seines lithophilen Charakters in geringen Mengen in fast allen silikatischen Gesteinen vertreten [7].
Die Thorium-Konzentration im Meerwasser ist um Größenordnungen geringer als die von Uran, eine Förderung aus Meerwasser ist somit in jedem Falle unwirtschaftlich.
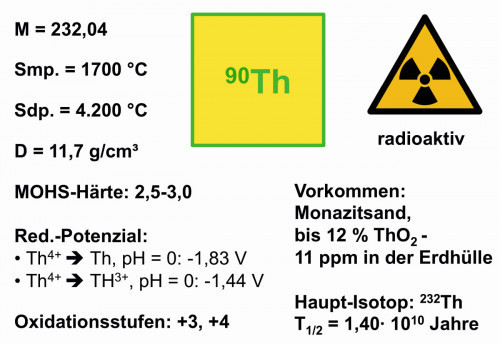 Abb. 3: Eigenschaften des Elements ThoriumThorium steht an 40. Stelle der Elementhäufigkeit und gehört zu den selteneren Elementen auf der Erde, denn es lässt sich weit verbreitet finden, tritt aber nur selten angereichert in größeren Mengen auf. In zahlreichen Mineralen ist es mit Uran, Blei oder Seltenerdmetallen vergesellschaftet. Monazit-Sande mit den Seltenen Erden sind die bedeutendsten Quellen für die Thorium-Gewinnung.
Abb. 3: Eigenschaften des Elements ThoriumThorium steht an 40. Stelle der Elementhäufigkeit und gehört zu den selteneren Elementen auf der Erde, denn es lässt sich weit verbreitet finden, tritt aber nur selten angereichert in größeren Mengen auf. In zahlreichen Mineralen ist es mit Uran, Blei oder Seltenerdmetallen vergesellschaftet. Monazit-Sande mit den Seltenen Erden sind die bedeutendsten Quellen für die Thorium-Gewinnung.
Monazit besteht aus etwa 60 % Cerphosphat, CePO4 sowie etwa und 1 bis 19 % Thoriumdioxid, ThO2. Thorium wurde seit Ende des 19. Jahrhunderts zu verschiedenen Verwendungszwecken aus Monazit isoliert.
Das radioaktive Metall wird in Australien, Norwegen, Sri Lanka, Kanada, USA, Indien, Lappland und Brasilien abgebaut. Stille Vorkommen von ca. 800.000 Tonnen liegen in der Türkei, überwiegend in der Provinz Eskişehir im Landkreis Sivrihisar.
Aufgrund der bekannten Geochemie des Thoriums kann auch in Deutschland mit Thorium-Lagerstätten gerechnet werden. Schließlich existieren auch hierzulande zahlreiche oberflächennahe oder sogar an der gegenwärtigen Landoberfläche freiliegende granitische Gesteine, Gneise und an manchen Stellen auch Aufarbeitungs-Produkte dieser Gesteine, welche sich in Sedimenten, wie z. B. in Sandsteinen wiederfinden. Darüber hinaus könnte die Suche nach Seifenlagerstätten fluviatiler Genese zu Thorium-haltigen Monazit-Vorkommen führen.
Der Geochemische Atlas von Sachsen zeigt die freistaatweite Verteilung zahlreicher Elemente in den oberflächennahen Gesteinen und Böden mit abbauwürdigen Thorium-Gehalten [8].
Der Weltmarktpreis für 1 kg Thorium lag zwischen 2008 und 2017 noch bei 60 US-$ [9, 10], ein Jahr später stand es bereits mit 162 US-$ auf der Preisliste der Elemente [11].
Erzaufarbeitung und Metall-Gewinnung
In den Mineralien der Erdrinde kann der Thorium-Gehalt schon an der Erdoberfläche durch Anwendung der Gammaspektroskopie anhand seines spezifischen Gammaspektrums mit hinreichender Genauigkeit detektiert werden. Dies gilt in jedem Fall ab Gehalten von einem Gramm je Tonne Gestein.
Das wirtschaftlichste Verfahren zur Thorium-Gewinnung ist der Aufschluss mit heißer Schwefelsäure bei über 200°C mit anschließender hydrolytischer Fällung durch Verdünnung mit Wasser. Problematisch sind das langsame Lösen der Mineral-Körner sowie die Komplexierung der gelösten Metall-Ionen durch Phosphate und Sulfate und die damit verbundenen unterschiedlichen VerfahrensParameter.
Ab etwa 1950 stieg das Interesse an Thorium höherer Reinheit für den Einsatz in nuklearen Prozessen. Der Schwefelsäure-Prozess erfuhr ergänzend eine Fällung mitOxalaten, die zu Thorium-Hydroxid umgesetzt werden. Da dieses Produkt noch mit Spuren von Selten Erd-Metallen verunreinigt ist, folgt eine Umsetzung mit Salpetersäure zu löslichen Nitraten. Mit Hilfe der Flüssig-flüssig-Extraktion von Thorium mit Tri-n-butyl-phosphat, TBP/ Kerosin, analog zum PUREX-Prozess, gelangt die Aufarbeitung zu reinem Thorium(IV)-nitrat, Th(NO3)4 [12].
Da Thorium eine geringe Elektronegativität von 1,3 auf der „Pauling-Skala“ besitzt, kann eine direkte Reduktion seiner Verbindungen nicht mit Hilfe von Kohlenstoff oder Wasserstoff erfolgen. Es würden sich hochschmelzende Thorium-Carbide oder -hydride bilden.
Zur Herstellung reinen Thorium-Metalls stehen vornehmlich drei Verfahren zur Verfügung:
- Die Schmelz-Elektrolyse von Thorium-Halogeniden in Salzbädern, wobei üblicherweise die Variationen KThF5 in NaCl, ThF4 in NaCl/ KCl oder ThCl4 in NaCl/ KCl zum Einsatz kommen
- Umsetzung mit unedlen Metallen: ThO2 mit Ca, ThCl4 mit Mg oder ThF4 mit Ca
- Die Gasphasentransport-Reaktion, die thermische Zersetzung von ThI4 nach dem Van-Arkel-de-Boer-Verfahren.
Die auf diese Weise gewonnenen Pulver oder „Metallschwämme“ werden unter Schutzgas oder im Vakuum zu massivem Material umgeschmolzen [13].
Verwendung des Thoriums
Aufgrund der Strahlen-Belastung wurden zahlreiche Anwendungen des Thoriums und seiner Verbindungen aufgegeben. Darunter fällt die Herstellung von Glühstrümpfen, die Nutzung als Röntgen-Kontrastmittel, der Einsatz des Thoriumdioxids für optische Gläser mit hohem Brechungsindex und das Zusetzen von 1 bis 4 % Thoriumdioxid zu Worfram-Inertgas-Schweißelektroden zur Verbesserung der Zündeigenschaften.
Geblieben sind die Konstruktion einer „Atomkern-Uhr“ mit angeregtem LASER-Licht mittels Thorium-229-Isotop, ein vom Europäischen Forschungsrat mit rund 14 Mio. Euro gefördertes Forschungsprojekt [14].
In den letzten Jahren erwuchs der Thorium-Salzschmelzreaktor zum neuen Hoffnungsträger für eine enorm reichhaltige und bändigbare Energie-Gewinnung, die von den fossilen Brennstoffen jeglicher Art unabhängig machen könnte.
Thorium-Reaktoren zur Energie-Gewinnung
Wie bereits in früheren Jahren amerikanische Atomphysiker zeigen konnten, lässt sich Thorium wesentlich gefahrloser und einfacher als herkömmliche Uran-Plutonium-Mischoxid-Reaktoren (MOX) zur Herstellung des spaltbaren Uranisotops233U verwenden.
Anders als im Uran-Plutonium-Brutreaktor, dem schnellen Brüter, ist dieses Verfahren auch in einem Reaktor möglich, bei dem die Kernspaltung durch thermische Neutronen erfolgt (Abb. 4). Das liegt am besonders hohen Wirkungsquerschnitt von 232Th für den Einfang eines thermischen Neutrons. Die erreichbaren Brutraten fallen bei einem solchen thermischen Brüter mit Thorium zwar geringer als beim schnellen Brüter aus, jedoch ist er wesentlich sicherer und ökonomischer zu betreiben.
 Abb. 4: 2030 soll der chinesische Thorium-Reaktor in Serie gehen (Foto: Commons, Stern)
Abb. 4: 2030 soll der chinesische Thorium-Reaktor in Serie gehen (Foto: Commons, Stern)
Durch Neutronen-Bestrahlung „erbrütet“ der Reaktor aus Thorium-232 das Thorium-233, das sich über Protactinium-233 mit den entsprechenden Halbwertszeiten unter Abgabe von Kernelektronen, den Beta-Strahlen, in Uran-233 umwandelt:
90Th-232 + 0n-1 → 90Th-233 - e- → 91Pa-233 - e → 92U-233.
Das Thorium mit dem Atomgewicht von 232 und 90 Protonen im Kern erhält durch Beschuss ein weiteres Neutron, wodurch sich das Atomgewicht auf 233 erhöht. Das aber gibt aus seinem Neutronen-Bestand ein Elektron ab, was zum Protactinium, Pa, mit 91 Protonen führt. Diese Elektronen- oder β-Strahlen-Emission vollzieht sich mit einer Halbwertszeit von 22,3 Minuten. Der entsprechende Schritt zum Uran-233 mit 92 Protonen verläuft mit einer Halbwertszeit von 26,967 Tagen, also fast einem Monat, deutlich langsamer.
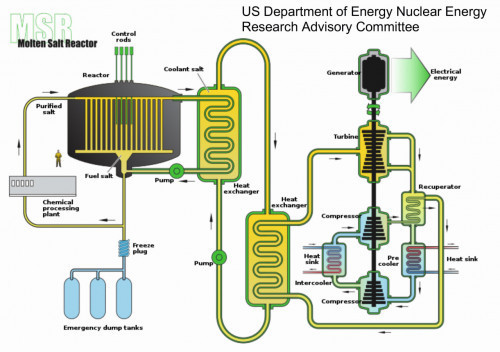
Da Thorium in größeren Mengen als Uran vorhanden ist, könnte es nach der zu erwartenden Abnahme der weltweiten Uranvorräte möglicherweise in Zukunft eine wichtige Energiequelle sein. Speziell im angelsächsischen Raum gab es Anfang der 2010er Jahre eine intensive Kampagne für eine Thorium-Nutzung zur angeblichen Lösung fast aller Energieprobleme [15]. Das Aufbau-Schema eines Flüssigsalz-Reaktors mit Thorium als Energiequelle zeigt Abbildung 5.
Neuere Studien weisen zudem darauf hin, dass eine Nukleartechnik unter Einbeziehung von Thorium erhebliche Proliferations-Risiken birgt [16]. Der Zugang zu Atombomben könnte für Terroristen erleichtert sein.
Als aktuelles Konzept für einen thermischen Brüter auf Thorium-Basis ist der „Flüssigsalzreaktor“ zu nennen [17], der bereits ab 2030 in China in Serie gehen soll.
Zurzeit wird vor allem in Indien Forschung zur Nutzung von Thorium in Kernkraftwerken betrieben, da in diesem Land die weltweit größten Thorium-Vorkommen zu finden sind [18].
Thorium-Verbindungen
In Übereinstimmung mit seiner Stellung im Periodensystem tritt Thorium in seinen Verbindungen normalerweise in der Oxidationsstufe +4 auf; Thorium(III)- und Thorium(II)-Verbindungen sind seltener.
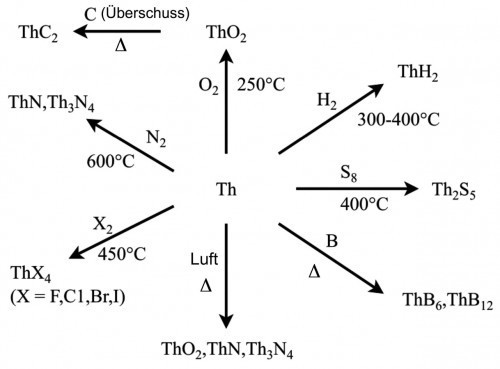
Die bedeutendste Verbindung ist das Thoriumdioxid, ThO2, das zu 6-8000 Euro/kg im Handel erwerbbar ist. Der Abbildung 6 sind die wichtigsten Reaktionen zur Herstellung von Präparaten aus dem Thoriummetall zu entnehmen.
Thoriumdioxid
Thorium(IV)-oxid oder Thoriumdioxid, ThO2, ist das einzige stabile Oxid des radioaktiven Elements und Actinoids Thorium, das in der Natur als Mineral „Thorianit“ vorkommt. Es ist ein farbloser kristalliner Feststoff von der Struktur des Calciumfluorits, CaF2.
Es lässt sich aus Thorium(IV)-hydroxid, Thorium(IV)oxalat, Thorium(IV)-carbonat oder Thorium(IV)-nitrat durch thermische Zersetzung leicht in reiner Form herstellen. Mit seinem Schmelzpunkt von 3.390 °C besitzt die Verbindung den höchsten aller Oxide. Die Dichte von
9,86 g/cm3 geht mit einem hohen Brechungsindex einher. Nur in stärkeren Säuren ist Thoriumdioxid löslich, in Wasser kaum. Die Radioaktivität von einem Gramm Thorium(IV)-oxid beträgt 7.100 Becquerel. Das heißt, 7.100 Alpha-Teilchen (Helium-Kerne) werden pro Sekunde emittiert[19].
Thorium-Dichalkogenide
Nach dem Thoriumdioxid steht das lilabraune bis purpurfarbene Thoriumdisulfid, ThS2, in der Reihe der Thorium-Dichalkogenide. Jedoch sind auch weitere Sulfide des Thoriums bekannt: das schwarze Thorium(II)-sulfid, ThS, das braune Thorium(III)-sulfid, Th2S3, das schwarze, Th7S12 (ThS1,71-ThS1,76), das tiefrote Polysulfid Th3S7 sowie das Thorium(IV)-oxidsulfid, ThOS [20, 21].
Das Thoriumdisulfid mit einem Molekulargewicht von 296,17 g/mol, einer Zersetzungstemperatur von etwa 1905 °C und einer Dichte von 7,36 g/cm3 bei Raumtemperatur kann als festes Schmiermittel Verwendung finden [22–24].
Das Thorium(IV)-selenid mit einem Molekulargewicht von 389.96 g/mol und einer Dichte von 8,5 g/cm3 bei Raumtemperatur steht auch als Sputter-Target für Oberflächen-Beschichtungen zur Verfügung [25].
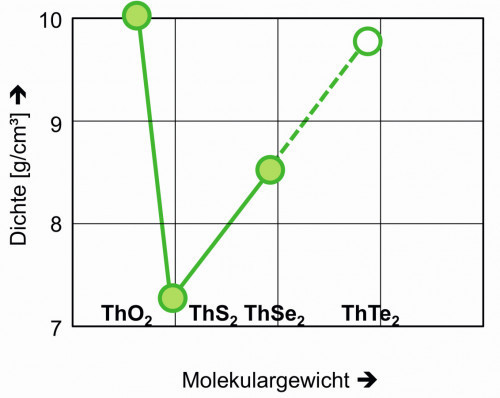
Mit gleicher Anwendung findet auch das Thorium(IV)tellurid, M = 487,24 gelegentlichen Einsatz. Seine Dichte wurde graphisch mittels Abbildung 7 mit 9,8 g/cm3 abgeschätzt.
Thoriumsulfate
Thorium(IV)-sulfat, Th(SO4)2, ist eine leicht wasserlösliche, farblose Verbindung mit einer Dichte von 4,255 g/cm3. Aus wässriger Lösung kristallisiert die Verbindung in Form von Hydraten, deren Wassergehalt von den Darstellungsbedingungen abhängt. Das Thoriumsulfat-Tetrahydrat Th(SO4)2 · 4 H2O kristallisiert in weißen Nadeln. Auch die Sulfate mit 8 und 9 Kristallwasser-Molekülen sind gut untersucht. Für das Sulfat mit 9 H2O wird bei 20 °C eine Löslichkeit von 13,8 g/L angegeben. Wasserfreies Thorium(IV)-sulfat erhält man beim Abrauchen von Thorium(IV)-oxid mit konz. Schwefelsäure [26]. Mit Alkalisulfaten bildet Thoriumsulfat in Wasser relativ schwerlösliche Sulfatothorate, wie z. B. Na2[Th(SO4)3] · n H2O, Na4[Th(SO4)4] · n H2O oder K6[Th(SO4)5] ·n H2O [27].
Thoriumnitrid und -nitrat
Thoriumnitrid, Th3N4, mit einem Molekulargewicht von 752,14g/mol und einer Dichte von 11,6 g/cm3 schmilzt erst bei 2.820 °C [26].
Thoriumnitrat, Th(NO3)4, ist eine farblose, leicht in Wasser und Ethanol lösliche chemische Verbindung und stellt ein wichtiges Zwischenprodukt bei der Darstellung von Thorium(IV)-oxid sowie von Thorium-Metall dar [27, 28]. Mit einem Molekulargewicht von 480,06 g/mol und einer Dichte von nur 2,78 g/cm3 zersetzt es sich bereits bei 50 °C unter Freigabe von Stickoxid-Gas und Sauerstoff:
Th(NO3)4 → ThO2 + 4 NO2 + O2.
Einst fand das Thoriumnitrat vielfachen Einsatz: Bei der Herstellung der Glühstrümpfe, für WIG-Schweißelektroden, Kathoden für Magnetron- und Wanderfeldröhren, als Ausgangsstoff für die damals als besonders gesund gehaltene Zahnpasta „Doramad“ sowie Badezusätze und Tinkturen, dievor allem gegen Ekzeme helfen sollten [29].
Thoriumhalogenide
Thorium(IV)-fluorid ist ein weißer Feststoff, der in Form eines kryptokristallinen Pulvers oder einfachbrechenden, schillernden Kristallen vorliegt. Er ist nahezu unlöslich in Wasser und besitzt eine monokline Kristallstruktur. Die Verbindung reagiert mit Luftfeuchtigkeit bei Temperaturen über 500 °C zu Thoriumoxidfluorid, ThOF2. Bei Darstellung aus Lösungen liegt es in Form von Hydraten vor, von denen das Hemihydrat das Einzige ist, von welchem die Struktur bekannt ist. Das Kristallwasser lässt sich aus dem Hemihydrat durch Erhitzung im Vakuum auf 400 °C entfernen [30].
Thorium(IV)-fluorid wird zur Herstellung von reinem Thorium und Hochtemperatur-Keramiken verwendet. Des Weiteren dient es als Sputter-Target zur Herstellung von Dünnschichten mit niedrigem Brechungsindex ohne Absorption im sichtbaren- und UV-Bereich. Auch bei der Herstellung von Kohlebogenlampen kommt es zum Einsatz.
Darüber hinaus laufen Versuche, Thorium(IV)-fluorid als Brennstoff für einen Flüssigfluorid-Thorium-Reaktor, LFTR, zu nutzen. Erste Exemplare dieser Reaktoren sind seit 2010 in Japan und seit 2014 in China in der Entwicklung [31].
Thorium(IV)-chlorid lässt sich durch Chlorierung von Thorium(IV)-oxalat mit einem Gemisch von Kohlendioxid und Tetrachlorkohlenstoff gewinnen sowie durch Reaktion von Thorium(IV)-oxid mit Kohlenstoff und Chlor oder mit Tetrachlorkohlenstoff alleine. Die Verbindung ist ein farbloser, hygroskopischer, kristalliner Feststoff, der zu großen Nadeln sublimiert. Neben einem Oktahydrat sind auch weitere Hydrate der Verbindung bekannt. Thorium(IV)-chlorid wird als Zwischenprodukt zur Herstellung von Thorium verwendet [32].
Thorium(IV)-bromid entsteht durch Reaktion von Thorium(IV)-oxid mit Brom und Kohlenstoff bei 800 bis 900°C. Das α-Thorium(IV)-bromid bildet sich bei längerem Erwärmen des Gemisches auf 330–375 °C. Reines β-Thorium(IV)-bromid entsteht beim Erwärmen auf 470 °C und Abschrecken in Eiswasser. Beide Modifikationen, von denen auch Hydrate bekannt sind, bilden weiße, kristalline, hygroskopische Verbindungen, die in Wasser, Ethanol und Essigester sehr gut löslich sind [33].
Thorium(IV)-iodid kann durch Reaktion von Thorium(IV)-carbid oder Thorium mit Iod bei 500 °C gewonnen werden. Des Weiteren ist eine Synthese mit Thorium(IV)-hydrid und Iodwasserstoff möglich:
ThH4 + 4 HI → ThI4 + 2 H2.
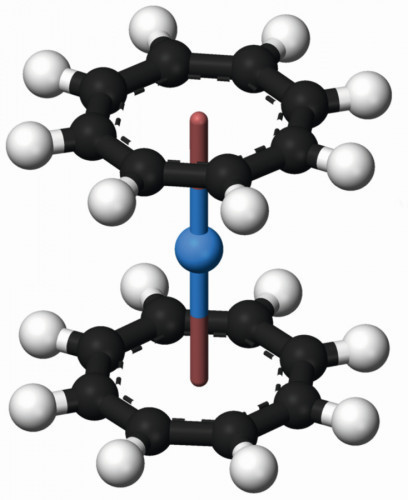 Abb. 9: Struktur des Thorocen, gelber Cyclooctatetraenid-Komplex, Th(C8H8)2Thorium(IV)-iodid ist ein äußerst luft- und feuchtigkeitsempfindlicher Feststoff, der in der Hitze in Form von orangefarbenen, in der Kälte als gelbe Kristallplättchen vorliegt. Es dient als Zwischenprodukt zur Herstellung von hochreinem Thorium durch thermische Zersetzung der Verbindung nach dem „Van-Arkel-de-Boer-Prozess“ [34].
Abb. 9: Struktur des Thorocen, gelber Cyclooctatetraenid-Komplex, Th(C8H8)2Thorium(IV)-iodid ist ein äußerst luft- und feuchtigkeitsempfindlicher Feststoff, der in der Hitze in Form von orangefarbenen, in der Kälte als gelbe Kristallplättchen vorliegt. Es dient als Zwischenprodukt zur Herstellung von hochreinem Thorium durch thermische Zersetzung der Verbindung nach dem „Van-Arkel-de-Boer-Prozess“ [34].
Daneben existieren schwarzes Thorium(II)-iodid in zwei hexagonalen Modifikationen (M = 612,75; Smp. = 850 °C (Z.); D = 7,21 g/cm3) [35] sowie das schwarze, violett-stichige, orthorhombische Thorium(III)-iodid (M = 612,75) [36].
Für die Analytik und Abtrennung des Thoriums von den Seltenerd-Metallen sind die Thiosulfat-Methode, die quantitative Fällung des Thoriums als Thoriumthiosulfat, Th(S2O3)2, aus neutralen Chlorid-Lösungen und die IodatMethode, die quantitative Fällung als Thoriumiodat, Th(IO3)4, aus stark salpetersauren Lösungen, zu nennen [37]. Schon in reinem Wasser löst sich das Iodat nur zu 0,369 g/L bei 20 °C [38].
Komplexe des Thoriums
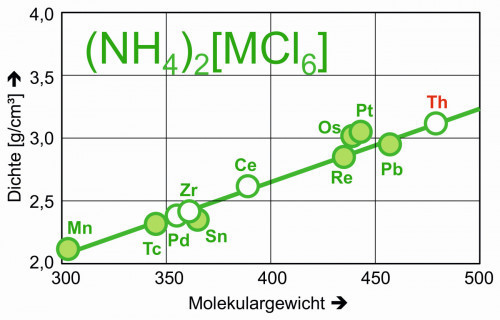
Das Thorium bildet analog zu anderen vierwertigen Zentralatomen auch Halogenido-Komplexe vom Typ [ThHal6]2-. Die Dichte von beispielsweise Ammoniumhexachloridothorat(IV), (NH4)2[ThCl6], lässt sich mit Hilfe analoger Verbindungen zu 3,1 g/cm3 abschätzen (Abb. 8).
Die meisten Arbeiten an Organothorium-Verbindungen konzentrieren sich auf die Sandwich-Strukturen der Cyclopentadienyle sowie Cyclooctatetraenyle (Abb. 9), die sich mit Thorium(IV)-fluorid und den Grignard-Verbindungen der Ring-Verbindungen herstellen lassen [18]. Sowohl zur quantitativen Analyse als auch zur Extraktion [39] kommt der Thorium-Komplex mit „Arsenazo III“, nach IUPAC: (3Z,6E)-3,6-bis[(2-arsenophyl)-hydrazinyliden]-4,5-dioxonaphthalen-2,7-Disulfonsäure (Abb. 10) zum Einsatz. Das UV-Spektrum des entsprechenden Thorium-Komplexes (Abb. 11) erlaubt die quantitative Analyse neben Uran und Seltenen Erden sowie einer Reihe weiterer Metalle [40].
Thorium in der Galvanotechnik
Das galvanische Abscheiden von Thorium aus Salzlösungen und Salzschmelzen ist hinlänglich bekannt und vielfach beschrieben [41]. Zumindest in der Patent-Literatur taucht das Galvanisieren von Thorium im Verbund mit anderen Metallen immer wieder auf [42].
Auch analytisch aus Abflüssen von Erzlagerstätten und anderen Abwässern lassen sich Spurenmetalle wie Thorium auf Graphit gut abscheiden und über die Radioaktivität quantitativ ermitteln [43].
Bei galvanischen Abscheidungen von Thorium hat sich besonders in Verbindung mit Edelmetall-Legierungen als sehr vorteilhaft erwiesen, dass diese eine hohe thermodynamische Stabilität gewährleisten. Untersuchungen an festen Palladium-Thorium-Schmelzen mit bis zu 16 Atom-% Thorium in Calciumfluorid-Elektrolytzellen bei 600 bis 800 °C zeigten eine außergewöhnliche Stabilität [44].
In den 1930iger Jahren nutzte die Fischer-Tropsch-Synthese zur Herstellung von Kohlenwasserstoffen aus Synthesegas (CO/ H2) ursprünglich einen Kobalt-Thorium-Katalysator [45], ein Verfahren, das heute wieder zur nachhaltigen galvanischen Anwendung gereichen könnte.
Sicherheit im Umgang mit Thorium und seinen Verbindungen
Thorium ist ein α-Strahler sowie im weiteren Verlauf des Zerfalls auch β-Strahler und aufgrund dieser Strahlungsarten bei Inhalation und Ingestion gefährlich. Metall-Stäube sowie vor allem Oxide sind aufgrund ihrer Lungengängigkeit radiotoxisch besonders riskant und können Krebs verursachen.
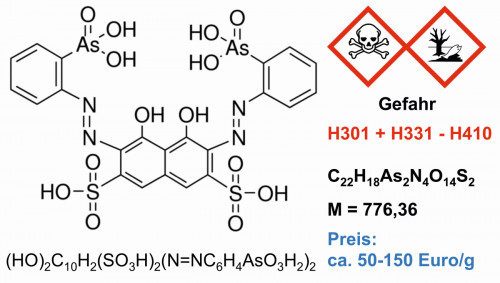 Abb. 11: UV-Spektren von Komplexbildner und Thorium-Komplex
Abb. 11: UV-Spektren von Komplexbildner und Thorium-Komplex
Einstufungen nach der CLP-Verordnung (Classification – Labelling – Packaging) [46] liegen nicht vor, weil diese nur die chemische Gefährlichkeit umfassen, die bei AlphaStrahlern wie Thorium und seinen Verbindungen eine völlig untergeordnete Rolle gegenüber der Radioaktivität und seinen gesundheitlichen Folgen spielt.
Die akute chemische Toxizität von Thorium und seinen Verbindungen wird von Toxikologen als gering eingeschätzt und im Wesentlichen auf die Radioaktivität zurückgeführt. Dies hängt mit der schlechten Wasserlöslichkeit von 0,0001 μg pro Liter des reinen Metalls sowie des meist vorkommenden Thoriumdioxids zusammen. Lediglich in sehr sauren Milieus ab einem pH-Wert < 4 sowie durch Komplexbildner löst sich Thorium in nennenswerten Mengen.
Das Thorium-Isotop Th-232 ist mit seiner Halbwertszeit von 14,05Mrd. Jahren noch wesentlich schwächer radioaktiv in seiner Dosis-Leistung als Uran-238, da durch die längere Halbwertszeit weniger Zerfälle pro Sekunde stattfinden und auch die Konzentration der kurzlebigen Zerfallsprodukte geringer bleibt. Als α-Emittent hat die Strahlung zwar eine geringe Reichweite, aber die Gefahr liegt beim Eindringen in den Körper.
Beim Lagern und Umgang mit Thorium und seinen Verbindungen ist auch die dauernde Anwesenheit der Elemente aus der Zerfallsreihe zu beachten. Besonders gefährlich sind die dabei auftretenden Beta- und die mit einem hohen 2,6-MeV-Anteil sehr energiereichen und durchdringungsfähigen Gammastrahlen [18].
Literatur
[1] Berzelius J. J.: Untersuchung eines neuen Minerals und einer darin enthaltenen zuvor unbekannten Erde, Annalen der Physik und Chemie, 92 (1829) 385–415
[2] Curie, M.: Rayons émis par les composés de l‘uranium et du thorium, Comptes rendus de l’Académie des sciences, 126 (1898) 1101–1103
[3] Badash, L.: The discovery of thorium’s radioactivity, Journal of Chemical Education, 43 (1966) 219–220
[4] https://de.wikipedia.org/wiki/Entdeckung_der_Radioaktivitaet
[5] Van Arkel, A.E; de Boer, J.H.: Darstellung von reinem Titanium-, Zirkonium-, Hafnium- und Thoriummetall, Z. anorg. allgem. Chem., 148/1 (1925) 345–350
[6] Lely, D. Jr.; Hamburger, L.: Herstellung der Elemente Thorium, Uran, Zirkon und Titan, Z. anorg. allgem. Chem., 87/1 (1914) 209–228
[7] Merkel, B.; Dudel, G. u. a.: Untersuchungen zur radiologischjen Emission des Uran-Tailings Schneckenstein, TU Bergakademie Freiburg und TU Dresden (1988)
[8] https://kipdf.com/thoriumlagerstaetten-weltweit-und-in-deutschland_5ac5f8141723dde15d5ac1bd.html
[9] https://www.final-frontier.ch/thoriumenergie
[10] https://www.mitsu-talk.de/forum/index.php?thread/57306-mit-8-gramm-100-jahre-fahren/
[11] http://www.leonland.de/elements_by_price/de/list
[12] https://de.wikipedia.org/wiki/PUREX-Prozess; PUREX = Plutonium-Uranium Recovery by Extraction
[13] Ullmann‘s Encyclopedia of industrial chemistry: Thorium, 8. Aufl. (2015)
[14] Seiferle, B. u. a.: Energy of the 229Th nuclear clock transition, Nature 573, (2019) 243–246
[15] Martin, R.: Super-Fuel: Thorium, the Green Energy Source for the Future, (2012)
[16] Thorium Report 2008, Oslo
[17] Ashley, S.F.; Parks, G.T.; Nuttall, W.J.; Boxall, C.; Grimes, R.W.: Thorium fuel has risks, Nature. Bd. 492/ 7427 (2012) 31–33
[18] https://de.wikipedia.org/wiki/Thorium
[19] https://de.wikipedia.org/wiki/Thorium(IV)-oxid
[20] https://wiki.edu.vn/wiki9/2020/12/12/verbindungen-von-thorium-wikipedia/
[21] Moscow Institute of Physics and Technology, MIPT (2020)
[22] Brauer, G. (Hrsg.): Handbuch der Präparativen Anorganischen Chemie, 3., umgearb. Aufl., Bd. II. Enke, Stuttgart (1978) 1148
[23] Perry D.L.: Handbook of Inorganic Compounds, Second Ed., CRC Press (2011) 489
[24] https://de.wikipedia.org/wiki/Thorium(IV)-sulfid
[25] https://www.americanelements.com/thorium-selenide-60763-24-8
[26] https://www.spektrum.de/lexikon/chemie/thorium-iv-sulfat/9238
[27] Brown, D. ; Wiedemeyer, H.: Th Thorium: Compounds with S, Se, Te, B Gmelin Handbook, Springer (2013) 63
[28] https://en.wikipedia.org/wiki/Thorium_compounds
[29] https://de.wikipedia.org/wiki/Thoriumnitrat
[30] https://de.wikipedia.org/wiki/Thorium(IV)-fluorid
[31] Odenwald, M: Garant für die Weltenergieversorgung, Focus online, 5. Mai (2011) 3
[32] https://de.wikipedia.org/wiki/Thorium(IV)-chlorid
[33] https://de.wikipedia.org/wiki/Thorium(IV)-bromid
[34] https://de.wikipedia.org/wiki/Thorium(IV)-iodid
[35] https://de.wikipedia.org/wiki/Thorium(II)-iodid
[36] https://de.wikipedia.org/wiki/Thorium(III)-iodid
[47] Proske, O. u. a.: Analyse der Metalle I – Schiedsverfahren, Springer, Berlin (1942) 125–127
[38] https://en.wikipedia.org/wiki/Solubility_table
[39] Zeinab F. Hegazy, M.A.: Selective cloud point extraction of thorium (IV) using tetraazonium based ionic liquid, Journal of Environmental Chemical Engeneering, Elsevier, 8/5 (2020)
[40] Fries, J. Getrost, H.: Organische Reagenzien für die Spurenanalyse, Merck, Darmstadt (1975) 352–353
[41] Müller, R.: Allgem. und techn. Elektrometallurgie, Springer, Wien (1932) 306
[42] https://patents.google.com/patent/DE1521063B2 (1974)
[43] https://www.dbu.de/OPAC/ab/DBU-Abschlussbericht-AZ-33285_01-Hauptbericht.pdf
[44] Schaller, H.-J.: Über die extrem hohe thermodynamische Stabilität von Pd-Th-Legierungen, Z. Naturforsch., 34 a (1979) 464–468
[45] https://de.wikipedia.org/wiki/Fischer-Tropsch-Synthese
[46] Europäische GHS Verordnung (EG) Nr. 1272/2008, genannt CLP-Verordnung (Classification, Labelling and Packaging), in Kraft getreten: 20. Januar 2009