 Mit der Richtlinie soll die Qualität und Rückverfolgbarkeit von Medizinprodukten erhöht werden. Dazu nimmt sie Einfluss auf die Prozesse in der Fertigung der Produkte und bringt zusätzlichen Prüf- und Dokumentationsaufwand mit sich. Denn die Zielsetzung der MDR, mit einwandfreien Medizinprodukten die Patienten- und Anwendersicherheit zu erhöhen, ist nur erreichbar, indem Hersteller von Medizinprodukten verpflichtet werden, alle relevanten regulatorischen Anforderungen zu erfüllen, bevor sie ihr Produkt auf den Markt bringen. Die Anforderungen beziehen sich dabei nicht nur auf das Medizinprodukt selbst. Darüber hinaus müssen auch die technische Dokumentation, die Klassifizierung, Zulassung sowie weitere Themen abgedeckt werden.
Mit der Richtlinie soll die Qualität und Rückverfolgbarkeit von Medizinprodukten erhöht werden. Dazu nimmt sie Einfluss auf die Prozesse in der Fertigung der Produkte und bringt zusätzlichen Prüf- und Dokumentationsaufwand mit sich. Denn die Zielsetzung der MDR, mit einwandfreien Medizinprodukten die Patienten- und Anwendersicherheit zu erhöhen, ist nur erreichbar, indem Hersteller von Medizinprodukten verpflichtet werden, alle relevanten regulatorischen Anforderungen zu erfüllen, bevor sie ihr Produkt auf den Markt bringen. Die Anforderungen beziehen sich dabei nicht nur auf das Medizinprodukt selbst. Darüber hinaus müssen auch die technische Dokumentation, die Klassifizierung, Zulassung sowie weitere Themen abgedeckt werden.
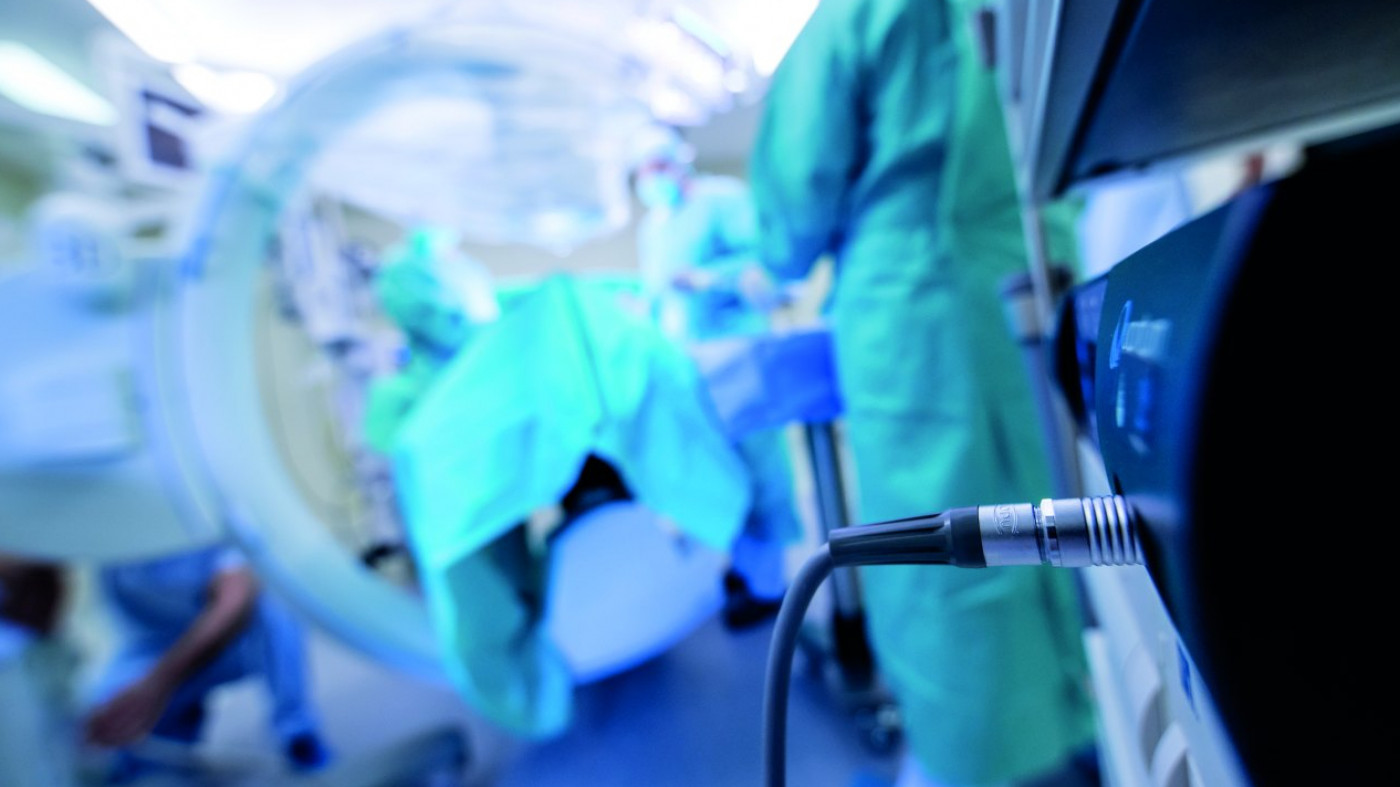
Hier sah sich deshalb auch ODU als Lieferant von Steckverbindungen für medizinische Applikationen in der Pflicht – denn Steckverbinder, Kabel und Gehäuse für Diagnostik, Therapie oder Monitoring sind relevante Teile von Medizinprodukten. Bereits als Vorprodukte müssen sie den Anforderungen der MDR entsprechen.
„Um unsere Kunden bei der vollständigen Technischen Dokumentation zu unterstützen, liegen bei uns nach DIN EN 13485:2016 zertifizierte Qualifizierungs- und Validierungs-Angaben vor“, so Mathias Wuttke, Business Development Manager für den Bereich Medizintechnik. Die Dokumente beinhalten Produktangaben in Form von technischen Datenblättern, Testberichten und Kennzeichnung von Produkten oder Baugruppen.
„Des Weiteren beachten wir als Firma ODU Themen wie Patienten- und Anwenderschutz unserer Produkte und setzen diese unter Einhaltung der IEC 60601-1 ein. Auch eine Umsetzung der Unique Device Identifikation (UDI) ist bei uns durch das Laserbeschriften unserer Stecker möglich“, so Wuttke. Auch im Falle von Änderungen an Produkten, die eine neue Risikobewertung erforderlich machen, kommuniziert der Zulieferer relevante Veränderungen an seine Kunden. „Dafür haben wir eigens eine Stelle im Unternehmen eingerichtet, die gezielt Anlaufstelle für Anfragen der Hersteller ist und Auskunft gibt.“
Der Beitrag des Steckverbinder-Spezialisten wird mit einem durchgängigen Risiko- und Qualitätsmanagementsystem erreicht und bietet entsprechende Unterstützung für die Kunden
- bei der lückenlosen Rückverfolgbarkeit
- bei der Post-Market Surveillance, um spätere, notwendige Korrektur- und Vorbeugemaßnahmen abzuleiten
- bei der Betrachtung des gesamten Produktlebenszyklus und
- für die verantwortliche Person des Inverkehrbringers und die Kunden aus der Medizin.
Das Unternehmen zählt zu den international führenden Anbietern von Steckverbindungssystemen und beschäftigt weltweit rund 2500 Mitarbeiter. Der Hauptsitz der ODU-Firmengruppe ist Mühldorf a. Inn. Weitere Produktions- und Produktentwicklungsstandorte sind in Sibiu/Rumänien, Shanghai/China, Tijuana/Mexiko und Camarillo/USA.
Das Unternehmen vereint unter einem Dach alle relevanten Kompetenzen und Schlüsseltechnologien für Konstruktion und Entwicklung, Werkzeug- und Sondermaschinenbau, Spritzerei, Stanzerei, Dreherei, Oberflächentechnik, Montage sowie Kabelkonfektionierung.
Die Firmengruppe ist mit ihren Produkten global vertreten und verfügt über ein internationales Vertriebsnetzwerk. Dazu gehören eigene Vertriebsgesellschaften in China, Dänemark, Deutschland, Frankreich, Hongkong, Italien, Japan, Korea, Rumänien, Schweden, UK und den USA sowie zahlreiche weltweite Vertriebspartner.
Steckverbindungen von ODU sorgen neben der Medizintechnik in zahlreichen weiteren anspruchsvollen Anwendungsbereichen für zuverlässige Übertragung von Leistung, Signalen, Daten und Medien – etwa in der Industrieelektronik oder Mess- und Prüftechnik, in Automotive-Anwendungen sowie bei Militär- und Sicherheitstechnik.