Die Metallisierung von Kunststoffen durch die Galvanik hat ein breites Anwendungsfeld. Dekor- und Zierelemente sowie Bedienkonzepte werden im Bereich des Automobilbaus, der Haushaltselektronik und Möbelindustrie gerne mit dieser Technologie umgesetzt.
UV-Peroxid-Behandlung
Abschließend ist die UV-H2O2-Oxidation als Vorbehandlungsmethode für das Chrom(III)-haltige Abwasser getestet worden. Hierfür ist eine Testanlage (s. Abb. 5) mit 15 L-Vorlagetank verwendet worden und nach verschiedenen Zeitabständen wurden Proben entnommen, welche anschließend durch Fällungsreaktion behandelt worden sind.
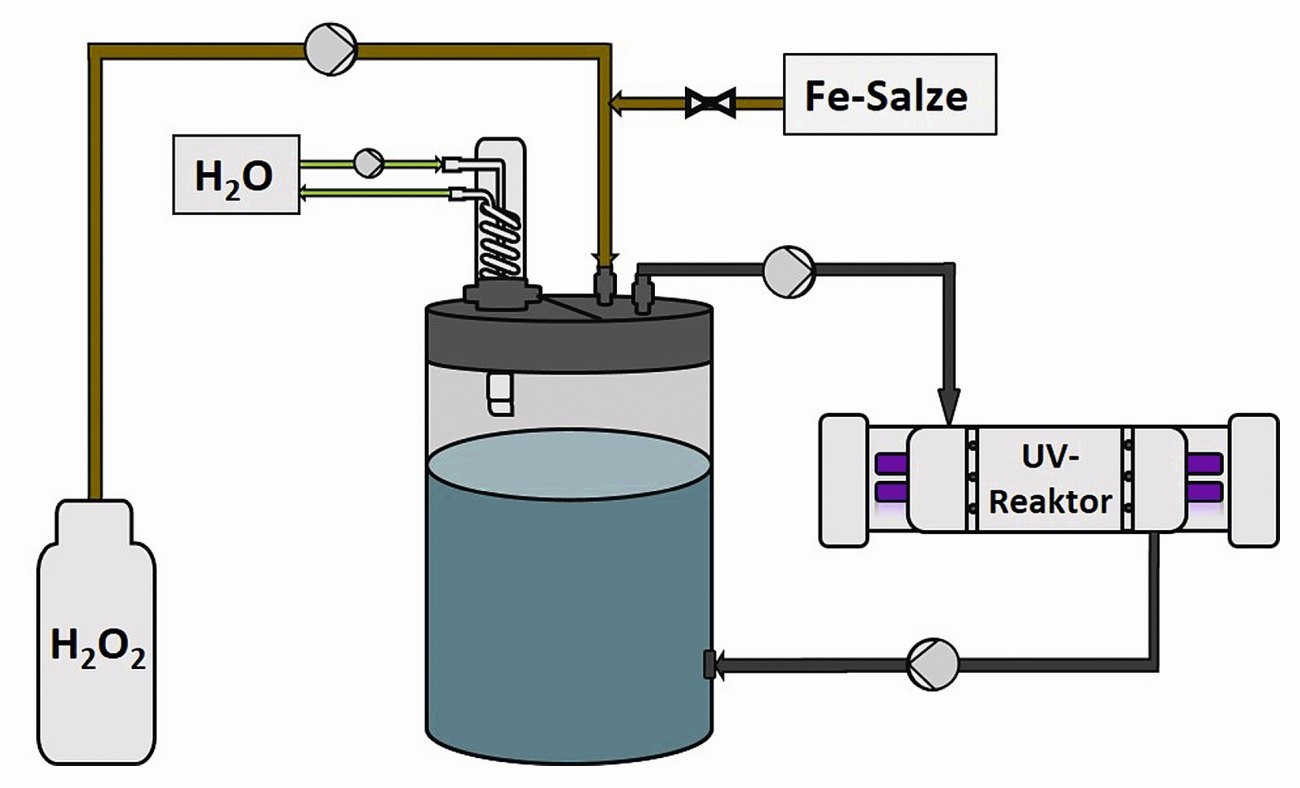 Abb. 5: Schematische Darstellung einer UV-Pilotanlage
Abb. 5: Schematische Darstellung einer UV-Pilotanlage
Der Mechanismus bei der UV-Peroxid-Oxidation beruht auf einer komplexen Radikalkettenreaktion. Durch das UV-Licht wird Wasserstoffperoxid homolytisch gespalten und dadurch Hydroxylradikale gebildet (s. Reaktionsgl. 1). Diese starken Oxidationsmittel reagieren mit den Chrom(III)-Komplexen sowie den freien Komplexbildnern. Eisensalze katalysieren die Reaktion.
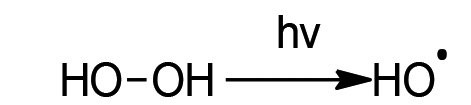 Reaktionsgl. 1: Homolytische Spaltung von Wasserstoffperoxid
Reaktionsgl. 1: Homolytische Spaltung von Wasserstoffperoxid
Hierfür ist im Versuch eine Fenton-Reagenz verwendet worden (bestehend aus Fe3+ und H2O2). Durch UV-Bestrahlung wird H2O2 homolytisch gespalten und gleichzeitig Eisen(III) zu Eisen(II) reduziert. Die entstandenen OH-Radikale sind sehr wichtige Oxidationsmittel und können schnell und unspezifisch mit fast allen organischen Verbindungen reagieren. In Kombination mit Sauerstoffmolekülen werden die organischen Verbindungen mineralisiert und letztendlich vollständig oxidiert [4].
Die entstandenen Chrom- und organischen Verbindungen im oxidierten Zustand mussten zunächst neutralisiert werden. Die Neutralisationsreaktion erfolgte mit einem geeigneten Reduktionsmittel und zuletzt wurden im alkalischen Bereich die Schwermetallhydroxide durch Fällungsmittel als Schlamm sedimentiert.
Nach der Behandlung des Chrom(III)-Abwassers konnte eine Reduktion des Chromgehaltes von 99,99% sowie eine Konzentration von 0,04-0,02 mg/L Chrom (gesamt) erreicht werden. Die Methode ist somit für beide getesteten Elektrolyte geeignet, um die gesetzlichen Grenzwerte einzuhalten.
- Zugabe von Reduktionsmittel
- Zugabe von NaOH
- Zugabe von Ca(OH)2
- Zugabe von NaAIO2
- Zugabe von Flockungshilfsmittel
- Filtrieren
Abb. 6: Behandlung einer Chrom(III)-haltigen Abwasserprobe mittels Hydroxidfällung nach der photochemischen Oxidation
Vergleich der Behandlungsmethoden
Für die Bestimmung der Chromkonzentrationen wurden Schnellküvetten Tests (UV-Messung) und ICP-OES Messungen durchgeführt. Dafür wurden die Chromkonzentrationen sowohl am Anfang vor der Behandlung als auch nach jedem Behandlungsverfahren untersucht. Die mittels ICP-OES-Messung bestimmten Werte werden in Tabelle 1 aufgelistet und darauffolgend in Abbildung 7, die prozentuale Reduktion aus den verschiedenen Verfahren dargestellt.
|
Verfahren |
Elektrolyt |
Chrom Ausgangskonzentration [mg/l] |
Chrom Endkonzentration [mg/l] |
Prozentuale Reduktion [%] |
|
I |
1 |
1.636 |
570,4 |
65,1 |
|
2 |
892,2 |
83,8 |
90,6 |
|
|
II |
1 |
816,9 |
24,8 |
97,0 |
|
2 |
949,4 |
14,3 |
98,5 |
|
|
III |
1 |
798,9 |
11,0 |
98,6 |
|
2 |
949,4 |
6,9 |
99,3 |
|
|
IV |
1 |
854,5 |
0,04 |
99,99 |
|
2 |
874,4 |
0,02 |
99,99 |
Aus Tabelle 1 ist zu erkennen: je höher die Ausgangskonzentration von Chrom(III)-haltigen Abwässern, desto schlechter lassen sich diese durch konventionelle Verfahren behandeln. Bei einer Chrom-Ausgangskonzentration von 1.636 mg/l ergab sich nach der Hydroxidfällung nur eine Chromreduktion von 65 %. Dieser Wert liegt so weit unterhalb der prozentualen Reduktion der weiteren Versuche, dass er für die Darstellung der Ergebnisse in Abbildung 7 nicht mehr berücksichtigt wurde.
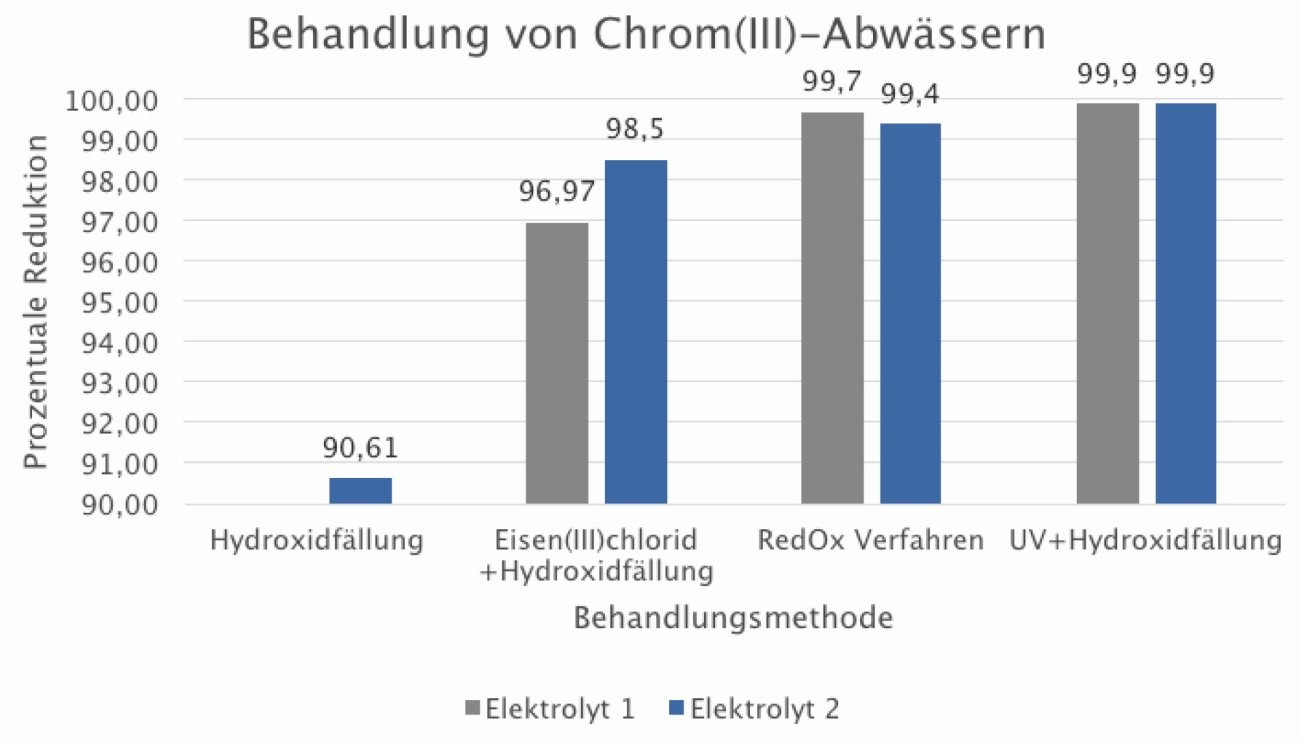 Abb. 7: Übersicht der prozentualen Reduktion von vier verschiedenen Verfahren zur Chrom(III)-Abwasserbehandlung
Abb. 7: Übersicht der prozentualen Reduktion von vier verschiedenen Verfahren zur Chrom(III)-Abwasserbehandlung
Die Ergebnisse aus Abbildung 7 zeigen die prozentuale Reduktion bei der Behandlung von 1 Liter Abwasserprobe mit einem pH-Wert von 10,5 nach den vier Methoden. Daraus lassen sich folgendene Schlüsse ableiten: Die hydroxydische Fällung funktioniert als Hilfsmittel, um die Konzentration von Chrom zu senken, allerdings reicht diese nicht für die gesetzlichen Vorgaben der AbwV Anhang 40 aus. Das Verfahren mittels Oxidations- und Reduktionsmitteln brachte im Vergleich zu der hydroxydischen Fällung eine deutliche Verringerung der Chromkonzentrationen. Trotz langer Reaktionszeiten und unterschiedlichen Chemikalien wurde der gesetzlich geforderte Chrom-Grenzwert nicht erreicht. Somit können auch diese Verbesserungen im Vergleich zur konventionellen Fällung nicht seriensicher und wirtschaftlich in der Produktion eingesetzt werden. Dies gilt zumindest bei Konzentrationen des Elektrolyten in der Spüle von ca. 10 %. Bei niedrigeren Konzentrationen kann die Behandlung nach Verfahren 3, ebenso wie nach Verfahren 2, ausreichend sein.
Gesetzeskonforme Ergebnisse
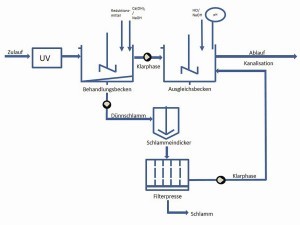 Abb. 8: UV-Behandlung und chemisch-mechanische Fällungsreaktion mit anschließendem Feinreinigungsschritt der behandelten Abwässer für die Einleitung in die KanalisationDas UV-Verfahren mit Wasserstoffperoxid und Eisen(III)-Salzen zeigte im Vergleich zu den ersten Versuchen, ein klar besseres Ergebnis. Bereits nach einer Behandlungszeit von 24 Stunden ließen sich die Komplexe soweit aufbrechen, dass nach der Behandlungszeit gesetzeskonforme Chrom-Konzentrationen in der Klarphase erzielt worden sind.
Abb. 8: UV-Behandlung und chemisch-mechanische Fällungsreaktion mit anschließendem Feinreinigungsschritt der behandelten Abwässer für die Einleitung in die KanalisationDas UV-Verfahren mit Wasserstoffperoxid und Eisen(III)-Salzen zeigte im Vergleich zu den ersten Versuchen, ein klar besseres Ergebnis. Bereits nach einer Behandlungszeit von 24 Stunden ließen sich die Komplexe soweit aufbrechen, dass nach der Behandlungszeit gesetzeskonforme Chrom-Konzentrationen in der Klarphase erzielt worden sind.
Abbildung 8 zeigt schematisch den Ablauf bei einer möglichen Behandlung von Chrom(III)-haltigen Abwässern mit einer UV-Anlage und anschließender Neutralisations-/Fällungsreaktion.
Abschließend erfolgt ein Abziehen der Klarphase und die Schlammphase wird über eine Kammerfilterpresse geleitet. Der Schlamm wird für die Entsorgung gesammelt und der Pressenauslauf sowie ggf. die Klarphase werden nach Passieren der Schlussfiltration in die Kanalisation einge- leitet.
Fazit:
Die dargestellten Analysen zeigen, dass eine sehr zuverlässige Spülwasserbehandlung von dreiwertigen Chromelektrolyten umgesetzt werden kann. Damit stellt ein Wechsel in der Beschichtung von sechswertigen auf dreiwertige Elektrolyte kein technisches Risiko in diesem Bereich dar, wenngleich wirtschaftlich die Kosten der Verfahren über denen der aktuellen Prozesse liegen. Im Bereich der eingesetzten Chemikalien, der resultierenden Schlamm-Menge sowie der erzielten Reduktion an Schwermetallen ist das UV-Peroxid-Verfahren aktuell eine sehr gute Wahl für die Produktion. Natürlich sind hier ebenfalls Investkosten sowie Betriebskosten zu betrachten, aber eine sichere und schnelle Behandlung ist mit diesem Verfahren möglich. Die klassischen Fällungen und der Einsatz von chemischen Oxidationsmitteln bieten aber Potential für weitere Entwicklungen. Sollten schwächere Komplexe in den Elektrolyten eingesetzt werden können, bieten auch diese Verfahren einen interessanten Ansatz.
[1] Europäische Chemikalienagentur (ECHA): Verordnung (EG) Nr. 1907/2006, URL https://echa.europa.eu/de/authorisation-list – Überprüfungsdatum 2021-01-11
[2] Bundesrepublik Deutschland: Gesetz zur Ordnung des Wasserhaushalts – Wasserhaushaltsgesetz (idF v. 31. 7. 2009), URL https://www.bgbl.de/xaver/bgbl/start.xav?startbk=Bundesanzeiger_BGBl&jumpTo=bgbl109s2585.pdf#__bgbl__%2F%2F*%5B%40attr_id%3D%27bgbl109s2585.pdf%27%5D_1610358307085 – Überprüfungsdatum 2021-01-11
[3] Gartiser, S.; Hafner, C.; Hercher, C.; Kronenberger-Schäfer, K.; Paschke, A.: Whole effluent assessment of industrial wastewater for determination of BAT compliance, Part 2: metal surface treatment industry (5)
[4] Peñafiel Ayala, R.: Photokatalytische Behandlung von biologisch schwer abbaubauren Wasserverunreinigung mit Titandioxid und simuliertem Sonnenlicht, Berlin, Technische Universität Berlin, genehmigte Dissertation, 2002






