Die Geschichte von Aluminium ist im Vergleich zu anderen Metallen, noch sehr jung. Vor weniger als 200 Jahren wurde auf der Weltausstellung in Paris im Jahre 1855 der erste Barren Rein-Aluminium präsentiert (Abb. 1). Kaiser Napoleon verwendete Aluminium Besteck nur zu ganz besonderen Anlässen, da es aufgrund der aufwendigen Herstellung aus Bauxit zur damaligen Zeit wie Gold gehandelt wurde. Abb. 1: Hier im Palais de l’Industrie wurde auf der Weltausstellung 1855 der erste Barren Rein-Aluminium präsentiert
Abb. 1: Hier im Palais de l’Industrie wurde auf der Weltausstellung 1855 der erste Barren Rein-Aluminium präsentiert
Heute hat sich Aluminium seinen Weg in viele Bereiche unseres Lebens erobert. Dank intensiver Forschung und zahllosen Anwendungsentwicklungen ist es gelungen das Leichtmetall Aluminium „salontauglich“ zu machen. Es ist vielfältig einsetzbar und aus unserem Alltag nicht mehr wegzudenken. Jeder von uns hatte bereits Kontakt mit diesem vielseitigen Werkstoff. Beim Öffnen einer Getränkedose, beim Reisen mit dem Flugzeug und dem Auto oder bei einer Trainingsfahrt mit dem Mountainbike.Im 19. Jahrhundert setzten intensive industrielle Entwicklungen ein, um metallisches Aluminium großtechnisch zu produzieren. Der Durchbruch gelang Ende des 19. Jahrhunderts durch die Entwicklung der Schmelzflusselektrolyse von Aluminiumoxid (Al2O3) von Paul L.T. Hérould und Charles M. Hall. Der österreichische Chemiker K.J. Bayer erforschte aus wirtschaftlichen und verfahrenstechnischen Gründen fast zeitgleich den Aufschluss von Bauxit zu Al2O3 mit Natronlauge. Dieser Prozess, bekannt als „Bayer-Verfahren“ ist auch heute noch im industriellen Einsatz.
Bauxit enthält Aluminiumoxid
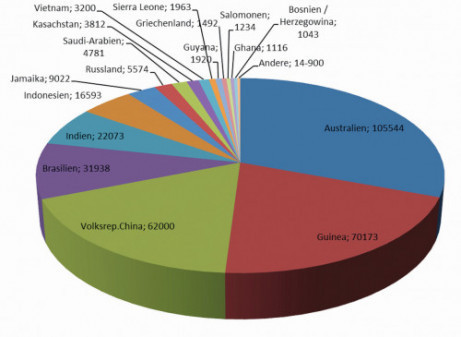
Aluminium ist mit ca. 8 % das dritthäufigste Element der Erdkruste. Jedoch kommt Aluminium nicht als Metall in der Erdkruste vor, sondern nur in gebundener Form. Bauxiterz, ein rötlich gefärbtes Sedimentgestein enthält einen großen Anteil an Aluminiumoxid, welches die Ausgangsbasis für die Aluminiumgewinnung darstellt (Abb. 2). Bauxit ist ein Rückstandsgestein, das durch die Verwitterung verschiedener Gesteine gebildet wurde. Die weltweit bekanntesten Bauxitvorkommen befinden sich an subtropischen und tropischen Standorten, wie Guinea, Mittel- und Südamerika, China, Indien und Australien (Abb. 3). Der Aluminiumgehalt der Bauxitvorkommen unterscheidet sich je nach Abbaugebiet und kann zwischen 40–55 % liegen. Der Aluminiumgehalt im Bauxit hat einen direkten Einfluss auf den für die Herstellung benötigten Aufwand an Energie. Je höherwertig der Aluminiumanteil im Bauxit ist, desto optimaler ist die Ertrags- und Aufwandsrechnung.
Zusammensetzung von Bauxit:
Bauxit ist ein Aluminiumerz, das für Aluminiumgewinnung annähernd folgende Zusammensetzung aufweist:
- Aluminium in Form von Aluminiumhydroxiden (Al(OH)3, AlO(OH))
- Eisenoxid Fe2O3
- Titanoxid TiO2
- Siliciumoxid SiO2
Aus Bauxit wird Tonerde – das Bayer-Verfahren
Im Bayer-Verfahren wird Aluminium als Hydroxid-Verbindung von den restlichen, im Bauxit vorkommenden, Mineralien getrennt. Dafür wird das Bauxiterz zuerst zerkleinert und gemahlen. Anschließend wird das Erz in Druckbehältern mit heißer Natronlauge und Kalk versetzt und unter Druck aufgeschlossen. Die Temperaturen für diesen Prozess liegen bei 120 bis 300 °C und bei Drücken von bis zu 200 bar. Die angewendeten Parameter hängen von der Art des Bauxits und der Anlagentechnik ab.
Aluminiumhydroxid ist weitestgehend gut in Natronlauge löslich. Es liegt in der Lösung als Natriumaluminatkomplex [Na(Al(OH)4)] vor. Die Lösung wird filtriert und von den nicht gelösten Bestandteilen getrennt. Der nicht gelöste Teil wird gewaschen und getrocknet und bildet den sogenannten Rotschlamm. Die eisenhaltigen Bestandteile führen zur charakteristischen Rotfärbung. Dieser muss in Rotschlammdeponien oder Schlammteichen sicher und umweltgerecht gelagert werden. Bei der Produktion einer Tonne Tonerde fallen ca. 0.5 bis 0.7 Tonnen Rotschlamm an.
Rotschlamm – ein gefährliches Nebenprodukt
Dieser wird auf große, eingedeichte und abgedichtete Deponien gepumpt. Die Rotschlammdeponie wird durch natürliche Trocknung gefestigt und kann mit einheimischen Pflanzen rekultiviert werden. Die Maßnahmen dauern einige Jahre, aber sie ermöglichen es, eine naturnahe Landschaft annähernd wieder herzustellen.
Die Lagerung des Rotschlamms ist jedoch auch ein umstrittenes Thema, da dieser in großen Schlammdeponien offen gelagert wird. Sind die Deponien nicht fachgerecht abgedichtet, können Unfälle passieren, wie im Jahre 2010 als der Damm eines Deponiebeckens der Aluminiumhütte MAL AG (Magyar Alumínium) im ungarischen Ajka brach. Es traten rund eine Millionen Kubikmeter des ätzenden und schwermetallhaltigen Schlamms aus. Etliche Menschen starben durch die Schlammflut oder wurden verletzt. Die Flora und Fauna wurde auf über 40 Quadratkilometern stark in Mitleidenschaft gezogen.
Schmelzflusselektrolyse nach Hall-Héroult
Die abgekühlte Natriumaluminatlösung wird durch Einsatz von festem Aluminiumhydroxid angeimpft und ausgefällt. Nach Filtration wird die flüssige Phase (Natronlauge) eingedampft und dem Aufschluss wieder zugeführt. Somit entsteht ein Kreislauf zur Wiederverwendung der Natronlauge. Das ausgefällte Aluminiumhydroxid wird mit Wasser gewaschen und Drehrohröfen bei Temperaturen von 1200 bis 1300 °C zu Aluminiumoxid kalziniert. Durch Abspaltung des Wasseranteils wird das Aluminiumhydrat in Aluminiumoxid umgewandelt.
2 Al(OH)3 → Al2O3 + 3 H2O
Das Aluminiumoxid, die sogenannte Tonerde hat eine Reinheit von 99,5 % und ist der Ausgangsstoff für die Herstellung von metallischem Aluminium. Eine Reduktion von Aluminiumoxid zu Aluminium erfolgt in einem elektrolytischen Prozess. Da Tonerde (Al2O3) einen Schmelzpunkt von > 2000 °C aufweist, wird die Tonerde in ein Kryolith Schmelzbad eingebracht. Kryolith Na3AlF6, sowie die verwendeten Fluorverbindungen Aluminiumfluorid AlF3 und Calciumfluorid CaF2 haben die Eigenschaft den Schmelzpunkt des Aluminiumoxids von über 2000 auf 950 bis 970 °C zu reduzieren. Zudem erhöhen die zugegebenen Salze die Leitfähigkeit der Schmelze.
Die Elektrolysezelle besteht aus einer feuerfest ausgekleideten Stahlwanne. Die zusätzliche Auskleidung durch Graphit oder Kohlenstoff dient als Kathode. Die Anoden bestehen meist aus Graphitzylindern und werden in die Schmelze eingetaucht. In der Schmelze liegt das Aluminiumoxid (Tonerde) als Al3+ und O2- Ionen vor. An der Kathode werden während der Schmelzflusselektrolyse Aluminiumionen zu metallischem Aluminium reduziert. Das Aluminium setzt sich am Zellenboden ab und wird regelmäßig unter Vakuum abgesaugt. Tonerde wird zugegeben um die Abscheidung im laufenden Prozess zu halten. Das abgeschiedene flüssige Aluminium besitzt eine Reinheit von > 99.5 % und kann durch weitere elektrochemische Prozesse auf 99.99 % gesteigert werden.
An der Graphitanode werden die Oxid-Ionen zu Sauerstoff oxidiert und reagieren mit der Kohlenstoff-Anode
zu Kohlenstoffmonoxid und Kohlenstoffdioxid. Durch diesen Reaktionsmechanismus werden die Graphitanoden verbraucht und müssen regelmäßig erneuert werden.
Die gesamte Redoxreaktion der Aluminiumherstellung (I) lässt sich in die Teilreaktionen die an der Kathode (II) bzw. Anode (III) ablaufen beschreiben:
(I) Gesamtreaktion
2 Al2O3 + 3 C → 4 Al + 3 CO2
(II)Reduktion an der Kathode
4 Al3+ + 12 e− → 4 Al
(III)Oxidation an der Anode
3 C + 6 O2 → 3 CO2 + 12 e−
Die treibende Kraft des Prozesses ist dabei der Umsatz von Elektronen, welcher durch das Anlegen einer Gleichspannung in Gang gesetzt wird. Die angelegte Spannung ist mit 4 bis 6 Volt relativ niedrig, jedoch ist der Stromfluss mit bis zu 300.000 Ampere sehr hoch.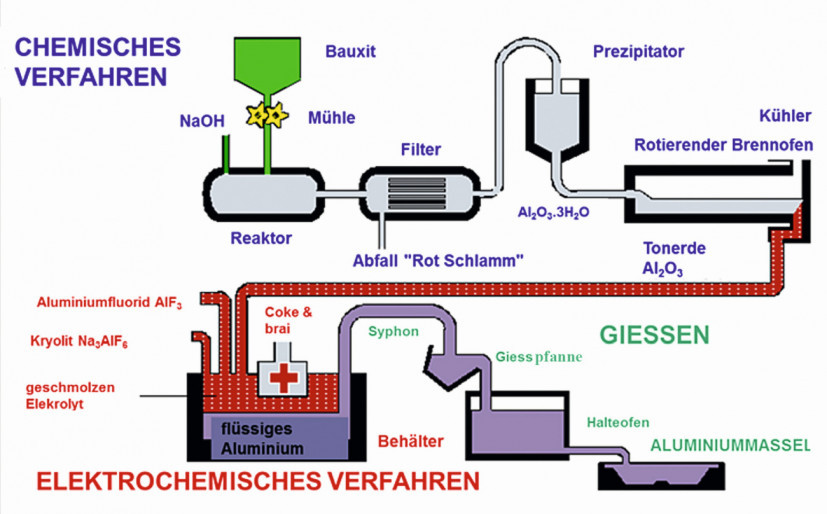 Abb. 4: Gesamtablauf der Aluminiumproduktion mit Bayerprozess und Schmelzelektrolyse/ Graphik: Constellium
Abb. 4: Gesamtablauf der Aluminiumproduktion mit Bayerprozess und Schmelzelektrolyse/ Graphik: Constellium
Die Grafik in Abbildung 4 zeigt schematisch im Überblick den Gesamtablauf der Aluminium-Produktion. Das chemische Verfahren (Bayer-Prozess) in der oberen Bildhälfte zeigt den Bauxitaufschluss mittels Natronlauge und die daraus resultierende Tonerdeproduktion. Die Tonerde ist der Ausgangsstoff für die Aluminiumproduktion mittels Elektrochemischem Verfahren (Schmelzelektrolyse) in der unteren Bildhälfte. Aus dem Schaubild ist ersichtlich, dass es sich um einen komplexen mehrstufigen Prozess handelt der auch einen hohen Energieumsatz erfordert.
Hoher Bedarf an Rohstoffen
Zur Herstellung von einer Tonne Aluminium (Abb. 5) werden vier Tonnen Bauxit und zwei Tonnen Tonerde benötigt. Zudem sind ca. 4 Kilogramm Kryolith und bis zu 20 Tonnen Aluminiumfluorid notwendig. Die Beschaffung des in der Natur nur selten vorkommenden Kryoliths ist sehr aufwendig, deshalb stellt man das Flussmittel aus Hexafluorokieselsäure her. Das Flussmittel wird im Kreislauf immer wieder eingesetzt, dadurch erklären sich auch die geringen Mengen. Die während des Prozesses entstehenden Abgase, wie Kohlenstoffdioxid und giftiges Kohlenstoffmonooxid, welche sehr aggressive Fluorverbindungen enthalten, werden gezielt abgesaugt. Die entstehenden Fluorverbindungen werden mit der eingeführten Tonerde adsorbiert und in den Kreislauf zurückgeführt.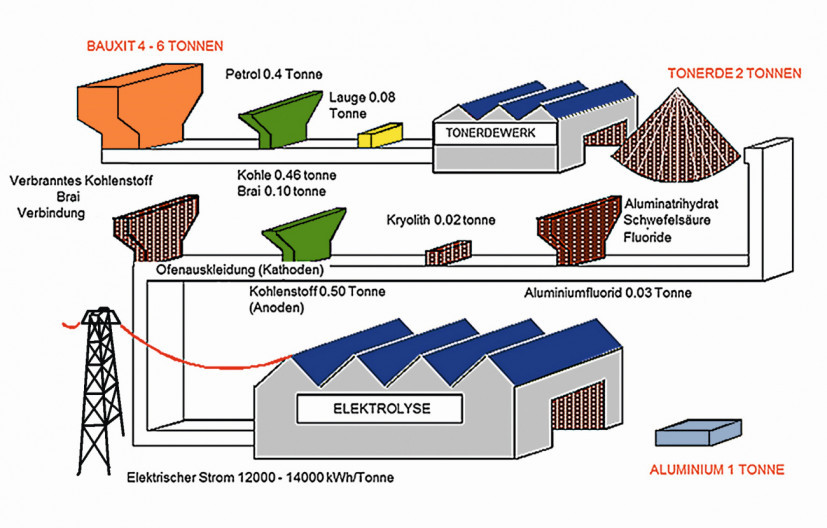 Abb. 5: Die Herstellung von Primäraluminium ist aufwendig und ressourcenintensiv, was dem Recycling in diesem Bereich besondere Bedeutung verleiht / Graphik: Constellium
Abb. 5: Die Herstellung von Primäraluminium ist aufwendig und ressourcenintensiv, was dem Recycling in diesem Bereich besondere Bedeutung verleiht / Graphik: Constellium
Aluminiumlegierungen
Das Aluminium wird in kleine Barren sog. Masseln gegossen. In den Aluminiumwerken werden durch Zugabe verschiedener Mineralien und Metalle wie z. B. Magnesium, Silicium, Zink oder Kupfer die gewünschten Aluminiumlegierungen hergestellt. Diese werden zu Walzbarren oder Pressbolzen vergossen und anschließend zu Platten, Blechen oder Profilen weiterverarbeitet. Die Herstellung von Primäraluminium ist mit einem sehr hohen Energieaufwand verbunden. Das aus dem Recycling von Aluminium hergestellte Sekundäraluminium lohnt sich deshalb aufgrund des deutlich geringeren Ressourcenaufwands.
Trotz der sehr energieaufwendigen Prozesse, metallisches Aluminium herzustellen, rechtfertigen die zahllosen Anwendungsmöglichkeiten verbunden mit den phantastischen Eigenschaften dieses Leichtmetalls diesen Aufwand.
Im nächsten Teil unserer Aluminiumserie geht es noch intensiver um Aluminiumlegierungen und um das Warm- und Kaltwalten des vielseitigen Leichtmetalls.